1. Điều trị ung thư không tế bào nhỏ
Ung thư phổi không tế bào nhỏ bao gồm ung thư biểu mô tế bào vảy, ung thư biểu mô tuyến, ung thư tế bào lớn và các khối u hỗn hợp. Cần lưu ý, đối với khối u hỗn hợp (nhiều typ ung thư trong một khối u) khi có mặt typ tế bào nhỏ thì phải xử lý như ung thư tế bào nhỏ .
1.1. Điều trị ung thư không tế bào nhỏ giai đoạn I, II, IIIA
1.1.1. Phẫu thuật
Phẫu thuật là một phương pháp chủ yếu để điều trị bệnh nhân ung thư phổi không tế bào nhỏ có phân loại lâm sàng TNM là giai đoạn I và II, không có di căn hoặc xâm lấn trung thất trước khi phẫu thuật .
Đối với bệnh nhân có thông khí phổi đạt tiêu chuẩn phẫu thuật, không có bệnh kèm theo nghiêm trọng, phẫu thuật cắt bỏ khối u là điều trị ban đầu hiệu quả nhất cho bệnh nhân giai đoạn I hoặc II .
Cắt thùy là phẫu thuật hiệu quả nhất. Cắt phổi hình chêm hoặc cắt phân thùy là lựa chọn tiếp theo. Căt phổi hoặc cắt bỏ nhiều thùy là cần thiết cho những khối u trung tâm không thể cắt thùy được .
Tỷ lệ tử vong liên quan đến phẫu thuật hiện nay khá thấp, tỷ lệ sống thêm được cải thiện rõ rệt tại các trung tâm phẫu thuật ung thư phổi trên thế giới .
- Cắt thùy phổi (Lobectomy):
Phẫu thuật cắt bỏ một thùy phổi là lựa chọn tối ưu cho ung thư phổi không tế bào nhỏ giai đoạn I, II vì bảo tồn được chức năng phổi .
Phẫu thuật cắt thùy qua nội soi lồng ngực (video videoassisted thoracoscopic - VATS) có thể là một giải pháp thay thế. Tuy nhiên, khối u trung tâm có thể không thể cắt thùy phổi dễ dàng, thường đòi hỏi phải cắt phổi rộng hơn, như cắt 2 thùy, thậm chí cắt phổi. Trong tình huống này, kỹ thuật cắt thùy nối khí-phế quản được ưa thích hơn cắt phổi (pneumonectomy) vì giữ được chức năng phổi tốt hơn và giảm các biến chứng của cắt phổi .
- Cắt phổi hạn chế:
Cắt phổi hạn chế gồm cắt phổi hình chêm và cắt phân thùy. Cắt phổi phân thùy là phẫu thuật được chỉ định cho những bệnh nhân không thể chịu đựng được phẫu thuật cắt thùy vì chức năng phổi kém, tuổi cao hoặc có các bệnh kết hợp nặng. Phẫu thuật này cắt bỏ một hoặc nhiều phân thùy phổi (segmentectomy) hoặc cắt phổi hình chêm không dựa trên giải phẫu phân thùy. Tiến bộ trong phẫu thuật qua nội soi lồng ngực làm tăng tỷ lệ được cắt bỏ khối u cho những bệnh nhân có các yếu tố nguy cơ cao nói trên .
So sánh kết quả sau mổ cho thấy cắt thùy có hiệu quả cao hơn so với cắt phổi hạn chế (phân thùy, hình chêm). Nghiên cứu của Mỹ (Study Group 801) trên 276 bệnh nhân ung thư phổi ngoại vi không tế bào nhỏ T1N0 (giai đoạn IA) cho thấy: tỷ lệ tái phát tại chỗ trong cắt phổi hạn chế cao gấp ba lần so với cắt thùy và tỷ lệ tử vong tăng 30%, đặc biệt ở bệnh nhân mô bệnh học không phải tế bào vảy .
Tuy nhiên, một phân tích hồi cứu dựa trên cơ sở dữ liệu SEER đã chứng minh rằng trong khi thời gian sống thêm của nhóm bệnh cắt phổi hạn chế thấp hơn đáng kể so với nhóm cắt thùy phổi đối với bệnh nhân dưới 74 tuổi; những người 74 tuổi trở lên không có sự khác biệt tồn tại giữa hai phương pháp phẫu thuật. Một số nghiên cứu khác đã chứng minh cắt phổi hạn chế kéo dài thời gian sống thêm ở nhóm bệnh khối u ngoại vi nhỏ cũng như ở nhóm ung thư tiểu phế quản-phế nang (bronchioloalveolar carcinoma) .
- Phẫu thuật qua nội soi lồng ngực (videoassisted thoracoscopic-VATS):
Phẫu thuật nội soi là một phương pháp ít xâm nhập để điều trị ung thư phổi không tế bào nhỏ giai đoạn I, II. Phẫu thuật nội soi làm giảm đáng kể biến chứng, tai biến của phẫu thuật, đặc biệt là biến chứng đau vùng mổ; là phẫu thuật rất thuận lợi cho những người có các bệnh kết hợp nặng. Tuy nhiên, phẫu thuật nội soi không nên chỉ định cho những khối u có đường kính > 3cm .
Do tỷ lệ biến chứng sau mổ rất thấp, nên bệnh nhân được phẫu thuật nội soi có thể tiếp nhận một cách thuận lợi trị liệu bổ trợ sau phẫu thuật (hóa chất, xạ trị). Một nghiên cứu cho thấy số bệnh nhân bị trì hoãn hóa trị sau mổ cắt phổi là 58%, trong khi ở nhóm phẫu thuật nội soi chỉ có 18%; tỷ lệ phải giảm liều hóa chất là 49% ở nhóm cắt phổi, nhưng chỉ có 26% ở nhóm phẫu thuật nội soi .
Nghiên cứu tại các trung tâm phẫu thuật lớn cũng đã khẳng định tính an toàn và hiệu quả cao của phẫu thuật nội soi trong cắt thùy phổi .
- Phẫu thuật ở những bệnh nhân có xâm lấn ung thư thành ngực:
Đối với bệnh nhân giai đoạn IIB (T3N0M0) có xâm lấn ung thư thành ngực, có thể chỉ định cắt toàn bộ khối (cắt khối u và cắt bỏ phần xân lấn thành ngực-enbloc). Một nghiên cứu trên 212 bệnh nhân cắt bỏ khối, tỷ lệ sống thêm 5 năm sau phẫu thuật là 40%. Nếu trong phẫu thuật xác định có di căn hạch thì tỷ lệ sống thêm 5 năm chỉ là 12% .
- Tỷ lệ tái phát tại chỗ:
Số liệu của nhiều nghiên cứu xác định tỷ lệ tái phát tại chỗ sau phẫu thuật cắt bỏ khối u trong ung thư không tế bào nhỏ giai đoạn I, II là 6%-55% .
Tổn thương tái phát thường thấy ở vùng kế cận khối u đã bị cắt bỏ, hạch rốn phổi trung thất cùng bên. Đây là những khu vực có thể xạ trị bổ trợ sau phẫu thuật .
Tỷ lệ tái phát tại chỗ sau 5 năm là 23%, thời gian tái phát trung bình là 14 tháng . Nguy cơ thất bại điều trị sau 5 năm là 42%, bao gồm cả tái phát tại tại chỗ và tái phát xa. Tỷ lệ thất bại điều trị do tái phát tại chỗ là 25%, do tái phát xa là 46% và phối hợp cả hai là 29% .
Các yếu tố nguy cơ tái phát tại chỗ bao gồm: cắt bỏ hình chêm, cắt phân thùy; mô bệnh học là ung thư tế bào dạng vảy hoặc tế bào lớn; giai đoạn bệnh IB, II hoặc IIIA .
1.1.2. Điều trị không phẫu thuật
Xạ trị có định vị hoặc điều trị bằng sóng radio tần số vô tuyến được chỉ định thay thế cho phẫu thuật đối với những bệnh nhân không có chỉ định phẫu thuật hoặc từ chối phẫu thuật .
a) Xạ trị:
Cho đến năm 2009 có 26 nghiên cứu ở những trung tâm xạ trị lớn nhất tại Bắc Mỹ và châu Âu nhằm đánh giá hiệu quả của xạ trị đối với 2000 bệnh nhân ung thư phổi không tế bào nhỏ giai đoạn I, II không phẫu thuật. Thời gian sống thêm toàn bộ 2, 3 và 5 năm tương ứng là 22%-72%, 17%-55% và 0-42%; thời gian sống thêm chỉ liên quan đến ung thư tương ứng là 54%-93%, 22%-56% và 13%-39%. Sau xạ trị, từ 11%-43% tử vong vì nguyên nhân không phải do ung thư. Rõ ràng, hiệu quả của phẫu thuật tốt hơn nhiều so với xạ trị đơn thuần: tỷ lệ sống thêm 2 và 5 năm sau phẫu thuật đạt tới 47%-67% .
Bệnh nhân được phẫu thuật sẽ được phân loại TNM trong phẫu thuật với độ chính xác cao hơn, do đó được điều trị bổ trợ phù hợp hơn sau phẫu thuật. Bệnh nhân không được phẫu thuật chỉ được đánh giá giai đoạn bằng lâm sàng ít chính xác hơn nhiều (thường sai sót tới 40%) nên không thể xây dựng được kế hoạch điều trị một cách chính xác .
Các kỹ thuật xạ trị mới:
- Xạ trị ba chiều (stereotactic body radiation therapy-SBRT): là một giải pháp thay thế đầy hứa hẹn cho những bệnh nhân từ chối phẫu thuật hoặc không có chỉ định phẫu thuật. Khác với xạ trị thông thường, kỹ thuật này bao gồm kế hoạch điều trị cố định và cực kỳ chính xác, do đó cho phép chiếu liều cao cho những khu vực tổn thương. Phương pháp này chỉ định cho những bệnh nhân có khối u nguyên phát nhỏ (< 3-4 cm) và chức năng phổi kém hoặc hoặc có bệnh kèm theo nặng chống chỉ định phẫu thuật cắt bỏ, vì vậy xạ trị ba chiều hoặc sóng điện từ tần số vô tuyến không phải là phương pháp điều trị triệt để nên cần cân nhắc khả năng phẫu thuật tối đa. Đối với những bệnh nhân có khối u nguyên phát lớn hơn và chức năng phổi kém hoặc có bệnh kèm theo nặng chống chỉ định phẫu thuật cắt bỏ thì xạ trị là chỉ định tuyệt đối .
- Phân liều chiếu (hyperfractionation): chiếu nhiều lần/ngày nhưng giảm liều mỗi lần chiếu có hiệu quả hơn so với chiếu một lần mỗi ngày. Ví dụ: xạ trị gia tốc liên tục phân liều chiếu (1,5Gy/lần x 3 lần/ngày trong 12 ngày liên tục; tổng liều 54Gy) hiệu quả hơn so với với nhóm xạ trị thông thường (1 lần/ngày trong 30 ngày, tổng liều 60Gy) .
- Xạ trị với bức xạ hạt nặng (heavy particle): chiếu bằng chùm proton hoặc ion cacbon được sử dụng trên cơ sở thử nghiệm ở bệnh nhân giai đoạn I. Kết quả sơ bộ cho thấy rằng những phương pháp này có thể mang lại kết quả tương tự với xạ trị thông thường .
b). Điều trị bằng sóng điện từ tần số vô tuyến: (radiofrequency ablation - RFA)
Sử dụng sóng điện từ phát ra từ một đầu dò được cấy bên trong khối u để tạo ra nhiệt, gây hoại tử khối u .
c). Điều trị hóa chất:
Nhằm mục đích giảm nguy cơ di căn xa và cải thiện thời gian sống thêm. Phẫu thuật phối hợp hóa trị bổ trợ cho các bệnh nhân giai đoạn IB , II và giai đoạn IIIA.
Điều trị hóa chất sau mổ
Nhiều thử nghiệm lâm sàng điều trị phác đồ 2 thuốc trong đó có nhóm platinum cho thấy có hiệu quả đối với bệnh nhân giai đoạn II và IB, những bệnh nhân với T2 có đường kính khối u > 4cm. Không điều trị hóa chất cho bệnh nhân giai đoạn IA. Các nghiên cứu cho thấy hóa trị bổ trợ dựa trên cisplatin thực sự bất lợi đối với bệnh nhân giai đoạn IA. Cũng có nhận xét rằng hóa trị bổ trợ cho bệnh nhân giai đoạn 1B có đường kính khối u < 4 cm có kết quả nghèo nàn hơn so với nhóm không điều trị bổ trợ .
Một số nghiên cứu bước đầu cho nhận xét những bệnh nhân giai đoạn I có biểu hiện gen hoặc phát hiện các dấu ấn methyl hóa ADN thì có nguy cơ tái phát cao hơn. Những bệnh nhân này nên điều trị bổ trợ sau mổ .
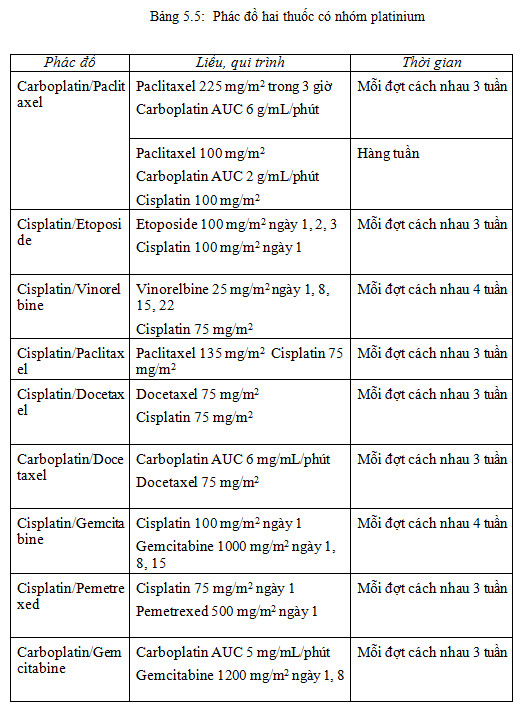
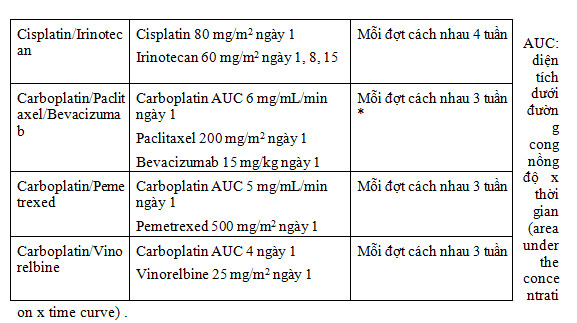
- Bevacizumab dùng 3 tuần/lần x 6 lần .
Phác đồ 3 thuốc không được khuyến cáo vì không cải thiện thời gian sống thêm; trái lại, làm tăng đáng kể tỷ lệ có tác dụng ngoại ý .
Không có phác đồ nào thể hiện hiệu quả tối ưu. Các thử nghiệm lâm sàng ngẫu nhiên cho thấy phác đồ dựa trên cisplatin có hiệu quả hơn phác đồ dựa trên sự kết hợp carboplatin hoặc phác đồ không có platinum .
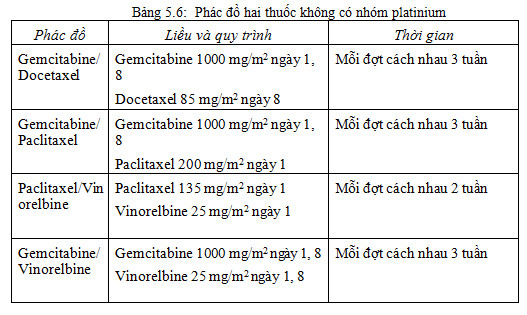
Bevacizumab, cetuximab
Sự phát triển khối u phụ thuộc vào hoạt động của các thụ thể bề mặt màng tế bào kiểm soát sự dẫn truyền tín hiệu vào trong tế bào và điều tiết phát triển tế bào, quá trình chết tự nhiên của tế bào, sự tăng sinh mạch cũng như sự bám dính và di cư của tế bào. Thụ thể yếu tố tăng trưởng biểu bì (epidermal growth factor receptor- EGFR), còn được gọi là HER1 hoặc erbB-1 tyrosine kinase (TKS) là thụ thể bề mặt tế bào. EGFR tồn tại như một chuỗi đơn (monomer) trên bề mặt tế bào có chức năng hoạt hóa tyrosine kinase (TK) .
Trong khi sự hoạt hóa TK của EGFR được kiểm soát chặt chẽ ở các tế bào bình thường thì gen mã hóa các thụ thể này đã bị khóa trong tế bào ác tính thông qua sự khuếch đại, sự bộc lộ quá mức hoặc do đột biến .
Gefitinib và erlotinib là các chất ức chế TK EGFR đầu tiên được sử dụng cho những bệnh nhân đã được điều trị bằng hóa trị liệu ban đầu. Đối với bệnh nhân có đột biến EGFR, có chỉ định tiến hành đơn trị liệu bằng thuốc ức chế EGFR TK (gefitinib, erlotinib) như là điều trị ban đầu đối với ung thư phổi không tế bào nhỏ. Chất ức chế TK EGFR phân tử nhỏ (gefitinib, erlotinib) đã được chứng minh có tác dụng kéo dài thời gian sống thêm ở bệnh nhân ung thư không tế bào nhỏ được điều trị hóa chất mặc dù có những tác dụng phụ nhất định .
Hiện nay, các kháng thể đơn dòng (bevacizumab, cetuximab) gắn với yếu tố tăng trưởng thụ thể biểu bì tyrosine kinase được sử dụng thay thế cho hóa trị hoặc kết hợp với hóa trị .
Chỉ định điều trị dựa trên kết quả xét nghiệm sịnh học phân tử và mô học của ung thư. Bệnh nhân phải được xét nghiệm hóa mô miễn dịch xác định sự hiện diện của một đột biến gen trong EGFR .
Nhiều nghiên cứu đã xác định những đối tượng bệnh nhân sau đây đáp ứng điều trị với các thuốc này, bao gồm: phụ nữ, người không hút thuốc, người Châu á, typ mô bệnh học là ung thư biểu mô dạng tuyến, các phân typ có nguy cơ cao đột biến EGFR. Tuy nhiên, để sử dụng TK EGFR cho bệnh nhân bắt buộc phải có xét nghiệm sinh học phân tử không được dựa vào lâm sàng đơn thuần .
Bevacizumab kết hợp hóa trị có kết quả điều trị tốt trong ung thư phổi không tế bào nhỏ không phải typ tế bào dạng vẩy, không có di căn não, không ho ra máu và không điều trị chống đông .
Đối với bệnh nhân ung thư phổi không tế bào nhỏ giai đoạn IV đang được hóa trị như là một phần của điều trị ban đầu, không có chỉ định sử dụng kết hợp một EGFR TK. Bevacizumab là một kháng thể đơn dòng có gắn yếu tố tăng trưởng nội mạc mạch (VEGF) .
Cetuximab là một kháng thể đơn dòng gắn vào các thụ thể yếu tố tăng trưởng biểu bì. Đối với bệnh nhân ung thư phổi không tế bào nhỏ có bộc lộ EGFR (xác định bằng hóa mô miễn dịch), chỉ định điều trị phối hợp cetuximab với phác đồ cisplatin cộng vinorelbine và phương pháp điều trị này có hiệu quả kéo dài thời gian sống thêm.
Các dược phẩm mới nói trên có thể sử dụng cho tất cả các giai đoạn bệnh cũng như các mức độ thể trạng toàn thân như liệu pháp đơn thuần hoặc kết hợp. Tuy nhiên, giá các dược phẩm này còn rất đắt, nên việc chỉ định ở nước ta còn rất hạn chế.
Điều trị bổ trợ ban đầu (Neoadjuvant chemotherrapy)
Nhiều nghiên cứu đánh giá hiệu quả của hóa trị bổ trợ trước phẫu thuật là kém. Hiện nay, các quan điểm điều trị nghiêng về sử dụng hóa trị bổ trợ sau phẫu thuật .
1.1.3. Xạ trị sau phẫu thuật
Xạ trị nhằm ngăn ngừa tái phát chỗ và cải thiện thời gian sống thêm .
Các nghiên cứu đều cho thấy tỷ lệ tái phát tại chỗ giảm ở nhóm bệnh nhân được xạ trị sau phẫu thuật. Tuy nhiên hiệu quả xạ trị liên quan đến kỹ thuật chiếu. Nếu chiếu phân đoạn liều thì kết quả tốt. Nếu chiếu liều hàng ngày thì kết quả thậm chí còn tồi hơn là không xạ trị bổ trợ .
1.2. Tiên lượng
Thời gian sống thêm trung bình khi có điều trị của giai đoạn IA, IB, IIA và IIB tương ứng là 59, 42, 34 và 23 tháng .
Ngoài hai yếu tố kích thước khối u và giai đoạn TNM, còn một số yếu tố ảnh hưởng đến kết quả điều trị, bao gồm:
- Typ mô bệnh học .
- Các dấu ấn phân tử .
- Bệnh kèm theo .
- Nơi điều trị .
1.2.1. Kích thước của khối u nguyên phát
Kích thước khối u nguyên phát ảnh hưởng trực tiếp đến tiên lượng. Tiên lượng luôn tốt hơn cho bệnh nhân giai đoạn IA được cắt bỏ khối u (khối u < 3cm) so với giai đoạn IB (khối u 3-7cm). Sự khác biệt về thời gian sống thêm 5 năm là 10%-20% .
Ngay trong giai đoạn IA, kích thước cũng ảnh hưởng đến tiên lượng. Những bệnh nhân khối u có kích thước < 1,5cm tiên lượng tốt hơn so với các khối u có kích thước 1,6cm-3,0cm (86% so với 79%). Số liệu này là cơ sở để xây dựng bảng phân loại lần thứ bảy của hệ thống TNM .
1.2.2. Mô bệnh học
Nhiều nghiên cứu đã cho kết quả trái ngược nhau, bằng chứng cho thấy mô bệnh học không phải là một yếu tố dự báo chi phối tiên lượng khi các biến số dự báo khác đều được xem xét .
1.2.3. Các dấu ấn phân tử (molecular markers)
Sự có mặt của đột biến trong các thụ thể yếu tố tăng trưởng biểu bì (EGFR) liên quan đến tiên lượng được cải thiện cũng như đáp ứng với các chất ức chế tyrosine kinase EGFR .
1.2.4. Bệnh kèm theo
Thời gian sống thêm ba năm giảm đi tương ứng với mức độ nghiêm trọng ngày càng tăng của bệnh kèm theo (tỷ lệ 86%, 75%, 69% và 70% tương ứng với không có bệnh kèm theo, mức độ nhẹ, trung bình và nghiêm trọng của bệnh kèm theo) .
1.2.5. Cơ sở y tế tiến hành phẫu thuật
Tỷ lệ tử vong thấp hơn đáng kể ở những trung tâm điều trị có số lượng bệnh nhân được phẫu thuật cao hơn. Số lượng bệnh nhân mổ tại bệnh viện cũng ảnh hưởng đến thời gian sống thêm 5 năm: thời gian sống thêm 5 năm kéo dài hơn khi bệnh nhân mổ ở những trung tâm có số ca mổ nhiều .
1.3. Theo dõi sau điều trị
Mục đích của theo dõi sau điều trị ban đầu là để phát hiện sớm tái phát để can thiệp có hiệu quả (tăng thời gian sống thêm, cải thiện chất lượng cuộc sống) .
Phương pháp theo dõi chủ động (chụp Xquang ngực ba tháng/lần, chụp CT-scans cộng với soi phế quản siêu âm sáu tháng/lần) có hiệu quả làm tăng tỷ lệ sống thêm trung bình từ khi phát hiện tái phát (19 so với 6 tháng) .
Hiện nay các tác giả đề nghị qui trình giám sát như sau: kiểm tra lâm sàng và chụp Xquang ngực ba tháng/lần trong hai năm đầu tiên sau khi điều trị ban đầu; trong 5 năm tiếp theo sau đó: cứ sáu tháng chụp Xquang ngực một lần. Từ năm thứ tám: CT-scans ngực được thay thế cho Xquang ngực mỗi năm một lần .
2. Điều trị ung thư tế bào nhỏ
- Chiến lược điều trị chủ yếu là hóa trị (điều trị hệ thống). Mặc dù ung thư phổi tế bào nhỏ đáp ứng cao đối với hóa trị và xạ trị, bệnh thường tái phát trong vòng vài tháng điều trị. Nếu không điều trị, thời gian sống thêm ngắn, thường chỉ được một vài tháng. Cải thiện chất lượng cuộc sống do hóa trị thể hiện ngay cả ở những bệnh nhân có bệnh kèm theo nặng .
+ Hiệu quả điều trị khác nhau tùy theo giai đoạn bệnh lúc chẩn đoán và có thể được tóm tắt như sau:
+ Đối với giai đoạn hạn chế: tỷ lệ đáp ứng tổng thể là 80%-90% với hóa trị kết hợp với xạ trị, bao gồm 50%-60% đáp ứng hoàn toàn .
+ Đối với giai đoạn lan rộng: 60%-80% đáp ứng với hóa trị, mặc dù đáp ứng hoàn toàn chỉ có 15%-20% .
- Xạ trị ngực cải thiện tỷ lệ kiểm soát địa phương từ 10 đến khoảng 40 đến 60 phần trăm trong giai đoạn khu trú, và được kết hợp với sự sống còn được cải thiện .
Thời gian sống thêm trung bình ngắn, thời gian trung bình 6-8 tháng trong hầu hết các báo cáo. Thời gian sống thêm trung bình từ thời điểm chẩn đoán, với giai đoạn khu trú là 14-20 tháng, với giai đoạn lan rộng là 8-13 tháng. Sau khi tái phát, thời gian sống thêm trung bình tồn tại khoảng bốn tháng .
Khoảng 20%-40% bệnh nhân giai đoạn khu trú tồn tại hai năm, giai đoạn lan rộng ít hơn khoảng 5%. Thời gian sống thêm ngoài 5 năm khoảng 10%-13% bệnh nhân .
2.1. Hóa trị
2.1.1. Nhiều tác nhân hóa học trị liệu có hoạt động đáng kể đối với ung thư tế bào nhỏ. Các nhóm thuốc quan trọng nhất bao gồm:
+ Nhóm Platinum (cisplatin, carboplatin) .
+ Nhóm podophyllotoxins (etoposide, teniposide) .
+ Nhóm camptothecins (irinotecan, topotecan) .
+ Nhóm alkylating (ifosfamide, cyclophosphamide) .
+ Nhóm anthracyclines (doxorubicin, epirubicin) .
+ Nhóm taxanes (paclitaxel, docetaxel) .
+ Vincristine .
Các nhóm thuốc ít sử dụng gồm: nitrosoureas, methotrexate, gemcitabine và vinorelbine .
Các nghiên cứu cho thấy hóa trị trong ung thư tế bào nhỏ có hiệu quả khi phối hợp thuốc, nhưng không có một phác đồ nào có hiệu quả nổi bật. Việc lựa chọn phác đồ dựa trên tác dụng, độc tính của các thuốc .
2.1.2. Đối với bệnh nhân giai đoạn khu trú
Nên dùng phác đồ kết hợp thuốc, trong đó có platinum, kết hợp với xạ trị lồng ngực đồng thời vào thời điểm tiến hành hóa trị đợt 1 hoặc 2. Nên dùng phác đồ cisplatin cộng etoposide (PE). Phác đồ này tương thích với kết hợp xạ trị đồng thời. Đối với những bệnh nhân đáp ứng hóa trị tốt, nên chiếu xạ sọ dự phòng .
2.1.3. Với bệnh nhân giai đoạn lan rộng
Hóa trị theo phác đồ kết hợp etoposide với carboplatin hoặc cisplatin. Các phác đồ thay thế etoposide bằng irinotecan, topotecan, hoặc epirubicin cũng có thể được lựa chọn .
Bệnh nhân cao tuổi được điều trị với các liều lượng tương tự và phác đồ như người trẻ, nếu điều kiện sức khỏe tổng thể của họ tốt .
Đối với bệnh nhân giai đoạn mở rộng đã hoàn thành hóa trị và đáp ứng tốt, nên chiếu xạ sọ dự phòng .
2.1.4. Phác đồ
- Phác đồ có nhóm platinum:
Đối với ung thư phổi tế bào nhỏ, phác đồ có platinum hiệu quả hơn phác đồ không có platinum. Điều này đã được chứng minh trong nhiều nghiên cứu. Tỷ lệ đáp ứng với điều trị đối với phác đồ có cisplatin cao hơn (69% ở phác đồ chứa cisplatin hoặc carboplatin so với 62% ở phác đồ không có platinum). Thời gian sống thêm 6 và 12 tháng tăng đáng kể (68% so với 66%) .
Cisplatin cộng etoposide (PE): Là phác đồ hay được sử dụng nhất. Trong nhiều nghiên cứu, phác đồ cisplatin cộng etoposide có hiệu quả như phác đồ cyclophosphamide, doxorubicin, vincristine (CDV) hoặc cyclophosphamide, epirubicin, và vincristine (CEV) nhưng có độc tính thấp hơn. Cả hai thuốc cisplatin và etoposide có độc tính với niêm mạc và huyết học thấp, nguy cơ viêm phổi kẽ hạn chế. Phác đồ cisplatin cộng etoposide thường được ưa dùng khi kết hợp hóa và xạ trị đối với ung thư tế bào nhỏ..
- Phác đồ carboplatin cộng etoposide:
Tại Hoa Kỳ, phác đồ carboplatin cộng etoposide được sử dụng nhiều nhất trong điều trị bệnh nhân ung thư tế bào nhỏ giai đoạn lan rộng vì độc tính thấp hơn, còn phác đồ cisplatin cộng etoposide được sử dụng cho bệnh nhân ung thư tế bào nhỏ giai đoạn khu trú vì tỷ lệ đáp ứng cao hơn .
- Phác đồ có irinotecan:
Nhiều thử nghiệm lâm sàng đánh giá hiệu quả của phác đồ có irinotecan tương tự camptothecin (thay thế cho etoposide) kết hợp với một hợp chất bạch kim cho thấy cải thiện kết quả đối với bệnh nhân ung thư tế bào nhỏ .
- Cisplatin cộng irinotecan:
Nghiên cứu của các tác giả Nhật Bản cho thấy sự kết hợp của cisplatin cộng irinotecan hiệu quả hơn cisplatin cộng etoposide. Trong thử nghiệm này phác đồ điều trị và kết quả như sau:
+ Cisplatin (80mg/m2 vào ngày 1) cộng với etoposide (100mg/m2 IV vàongày 1 đến 3) mỗi ba tuần. Tỷ lệ đáp ứng 84%, tỷ lệ sống thêm 2 năm 19,5%. Mặc dù độc tính huyết học ít, irinotecan gây ra tiêu chảy nhiều hơn .
+ Cisplatin (60mg/m2 vào ngày 1) cộng với irinotecan (60mg/m2 vào các ngày 1, 8, và 15) bốn tuần một đợt. Tỷ lệ đáp ứng 84%, tỷ lệ sống thêm 2 năm 19,5%. Tỷ lệ đáp ứng 68%, tỷ lệ sống thêm 2 năm 5,2% .
Kết quả trên rất đáng khích lệ. Tuy nhiên, các thử nghiệm lâm sàng tại Hoa Kỳ lại không xác nhận phát hiện này, do đó cần phải có đánh giá tiếp về phác đồ này .
+ Carboplatin cộng irinotecan: Kết quả nghiên cứu cho thấy irinotecan có thể thay thế cho etoposide trong phác đồ kết hợp với carboplatin. Nhìn chung tỷ lệ sống thêm cao hơn so với phác đồ có etoposide .
- Topotecan cộng với cisplatin:
Các topotecan camptothecin đang được sử dụng điều trị ung thư tế bào nhỏ, tiêm tĩnh mạch topotecan là lựa chọn điều trị cho bệnh nhân tái phát và nhạy cảm với hóa trị .
Topotecan đã được kết hợp với nhiều loại thuốc khác trong điều trị ban đầu ung thư tế bào nhỏ, nhưng đã không chứng minh được hiệu quả cao hơn phác đồ platinum-etoposide .
- Epirubicin cộng với cisplatin:
Dùng etoposide có lợi bệnh nhân, cho phép đợt điều trị chỉ trong một ngày. Phác đồ epirubicin epirubicin và cisplatin như sau: epirubicin (100 mg/m2 vào ngày 1) và cisplatin (100 mg/m2 vào ngày 1), các đợt điều trị cách nhau ba tuần .
- Phác đồ ba thuốc:
+ Paclitaxel:
Bổ sung thêm paclitaxel cho phác đồ platinum cộng etoposide (PE) không cho hiệu quả rõ ràng mặc dù có cải thiện thời gian sống thêm nhưng không tăng tỷ lệ đáp ứng điều trị .
Dựa trên các kết quả nghiên cứu hiện nay, việc bổ sung paclitaxel cho phác đồ PE đối với bệnh nhân giai đoạn khu trú hoặc lan rộng chỉ nên được xem xét trong bối cảnh của một thử nghiệm lâm sàng .
+ Ifosfamide:
Lợi ích của việc bổ sung ifosfamide với PE không rõ ràng. Đã có một thử nghiệm lâm sàng so sánh phác đồ PE có và không có ifosfamide ở 171 bệnh nhân giai đoạn lan rộng cho thấy kéo dài thời gian sống thêm .
- Phác đồ 4 thuốc:
Tuy tỷ lệ đáp ứng cao hơn nhưng không kéo dài thời gian sống thêm. Tuy nhiên, độc tính xuất hiện nhiều khi sử dụng phác đồ 4 thuốc. Điều này đã được xác định trong một thử nghiệm lâm sàng do Viện ung thư của Pháp tiến hành trên 226 bệnh nhân giai đoạn lan rộng với phác đồ: etoposide (100 mg/m2 vào ngày 1 đến 3), cisplatin (100 mg/m2 vào ngày thứ 2), cyclophosphamide (400 mg/m2 vào ngày 1 đến 3) và epirubicin (40 mg/m2 vào ngày 1), dùng 6 đợt, mỗi đợt cách nhau 4 tuần. Tỷ lệ đáp ứng là 76%, tỷ lệ sống thêm trung bình 10,5 tháng, tỷ lệ sống thêm 1 năm đạt 40%. Tỷ lệ độc tính huyết học, đặc biệt là sốt, giảm bạch cầu, cũng cao hơn đáng kể tới 70%, tỷ lệ phải truyền khối hồng cầu là 45%, truyền khối tiểu cầu là 38%. Tỷ lệ tử vong hầu như không được cải thiện .
- Phác đồ xen kẽ:
Việc không thể cải thiện thời gian sống thêm mặc dù khối u nhạy cảm với hóa trị ban đầu cho thấy có một số lượng nhỏ các tế bào khối u đó đã kháng thuốc. Để khắc phục sự kháng thuốc, "không kháng chéo", liệu pháp kết hợp xen kẽ các phác đồ khác nhau đã được sử dụng trong điều trị ung thư phổi tế bào nhỏ ở cả giai đoạn khu trú và lan rộng .
Các phác đồ được sử dụng bao gồm:
+ Phác đồ CAV với PE .
+ Phác đồ CDE với VIMP (vincristine, carboplatin, ifosfamide và mesna) .
+ Phác đồ PE với topotecan .
Tuy nhiên hiệu quả của các thử nghiệm này đã không chứng minh được và việc sử dụng xen kẽ các phác đồ cần phải tiếp tục nghiên cứu, chưa thể ứng dụng lâm sàng.
- Tăng liều điều trị:
Các nghiên cứu tiền lâm sàng đã khẳng định có mối quan hệ giữa liều lượng và đáp ứng điều trị đối với một số loại thuốc .
Các biện pháp tăng liều hóa chất bao gồm:
+ Tăng liều thuốc cho một đợt (một chu kỳ) điều trị .
+ Tăng số đợt điều trị .
+ Giảm thời gian giữa các thuốc hoặc các đợt điều trị .
Khi áp dụng các biện pháp tăng liều nói trên phải sử dụng thuốc tăng bạch cầu; có thể phải sử dụng phương pháp điều trị tiếp theo là hoàn nguyên tủy xương với tế bào gốc tạo máu tự thân .
Tăng liều trong quá trình điều trị :
Một trong những phương pháp đơn giản nhất để khắc phục kháng thuốc là tăng dần liều thuốc đến mức mỗi bệnh nhân có thể dung nạp được mà không diệt tủy (không cần cấy tế bào gốc). Kết quả của tất cả các thử nghiệm lâm sàng cho thấy tăng dần liều thuốc đã làm tăng cao tỷ lệ đáp ứng thuốc so với khi dùng liều chuẩn. Tuy nhiên, tỷ lệ xuất hiện độc tính thuốc cũng tăng lên nhiều; ngoài ra, hầu hết các thử nghiệm đã không chứng minh được hiệu quả tăng thời gian sống thêm của bệnh nhân. Vì vậy, hiện nay chưa nên áp dụng phương pháp điều trị này, cần có những nghiên cứu đánh giá cụ thể hơn .
2.2. Điều trị hỗ trợ bằng các cytokine
Liều hóa chất có thể tăng cao hơn khi dùng kèm theo các cytokin kích thích tăng trưởng tế bào máu, ví dụ: yếu tố kích thíc xâm lấn đại thực bào-bạch cầu hạt (granulocyte-macrophage colony stimulating factor-GM-CSF); yếu tố kích thích xâm lấn bạch cầu hạt G-CSF). Nhưng lưu ý không được tăng liều lượng CSF vì không cải thiện thêm hiệu quả điều trị và xuất hiện nhiều tác động bất lợi cho bệnh nhân .
Không sử dụng các yếu tố tăng trưởng tế bào máu cho bệnh nhân đang xạ trị gây giảm tiểu cầu nặng, kéo dài thời gian điều trị nội trú, phải sử dụng kháng sinh tiêm và truyền máu nhiều hơn, tỷ lệ tử vong do tác dụng phụ tăng .
2.3. Cấy ghép tế bào tạo máu
Hiện nay đang quá trình thử nghiệm cấy ghép tế bào tạo máu sau khi điều trị hóa chất liều cao (gây diệt tủy). Mặc dù có một số kết quả ban đầu nhưng còn cần nhiều thời gian nữa để đưa ra qui trình cụ thể và đánh giá hiệu quả điều trị chính xác hơn .
2.4. Phẫu thuật điều trị ung thư phổi tế bào nhỏ
Tại thời điểm hiện tại, phẫu thuật không được chỉ định cho phần lớn bệnh nhân ung thư phổi tế bào nhỏ. Tuy nhiên, phẫu thuật cắt bỏ khối u giai đoạn khu trú dạng u tròn đơn độc trước khi hóa trị là một lựa chọn hợp lý. Không nên phẫu thuật sau hóa trị vì các nghiên cứu đã xác định kết quả bất lợi của phương thức điều trị này. Hóa trị và xạ trị sau phẫu thuật tiến hành như đã nêu ở trên .
2.5. Xạ trị trong ung thư tế bào nhỏ
Phương thức điều trị tối ưu ung thư phổi tế bào nhỏ giai đoạn hạn chế là phối hợp hóa trị và xạ trị lồng ngực .
Xạ trị nên tiến hành đồng thời với hóa trị liệu, không nên tiến hành sau khi hoàn thành hóa trị. Thời điểm bắt đầu xạ trị được khuyến cáo vào chu kỳ thứ nhất hoặc thứ hai của hóa trị và chiếu vào những ngày không điều trị hóa chất .
Có nhiều phác đồ xạ trị. Các phác đồ được nhiều trung tâm ứng dụng hiện nay như sau: tổng liều chiếu 45 Gy, phân liều chiếu hai lần mỗi ngày, chiếu 5 ngày/tuần, thời gian điều trị là ba tuần. Nếu phác đồ này không khả thi thì lựa chọn phác đồ sau: chiếu với liều 1,8-2,0 Gy/lần, mỗi ngày một lần, chiếu 5 ngày/tuần với tổng liều chiếu 60-70 Gy. Mô đích là khối u nguyên phát, các hạch bạch huyết đã xác định được bằng CT-scans .
Chiếu xạ sọ dự phòng làm giảm tỷ lệ di căn não và kéo dài thời gian sống thêm đối với bệnh nhân ung thư tế bào nhỏ. Phương pháp điều trị này có chỉ định như sau:
- Bệnh nhân ung thư tế bào nhỏ giai đoạn khu trú đáp ứng hoàn toàn hoặc không hoàn toàn với điều trị ban đầu (hóa trị kết hợp xạ trị) .
- Bệnh nhân ung thư tế bào nhỏ giai đoạn lan rộng đã đáp ứng hoàn toàn với điều trị ban đầu và tình trạng toàn thân tốt .
Liệu trình điều trị: tổng liều chiếu là 30 Gy, liều một lần chiếu là 2 Gy; hoặc tổng liều 25Gy, liều mỗi lần chiếu 2,5Gy .
3 ĐIỀU TRỊ GIẢM NHẸ TRONG UNG THƯ PHỔI
- Chiếu xạ những tổn thương trong lồng ngực tiến triển hoặc các di căn (ví dụ, xương, não) .
- Điều trị di căn xương: di căn xương làm giảm chất lượng cuộc sống do gây đau hoặc gây gãy xương bệnh lý. Liệu pháp bisphosphonate chỉ định cho bệnh nhân ung thư không tế bào nhỏ di căn xương. Acid zoledronic (tên thương mại Zometa, Zomera, Aclasta và Reclast) giảm đáng kể các biến chứng do di căn xương (gãy xương bệnh lý, lún cột sống, tăng calci huyết) .
Cách dùng
Zoledronate liều lượng chuẩn 4mg, truyền tĩnh mạch trong 15 phút, 1 lần/tháng .
Tác dụng phụ: mệt mỏi, thiếu máu, đau cơ, sốt, sưng chân. Triệu chứng giống cúm thường gặp sau khi truyền lần đầu tiên. Zoledronate nhanh chóng thải trừ qua thận, do đó không nên dùng cho bệnh nhân có chức năng thận giảm hoặc bệnh thận. Một biến chứng hiếm gặp ở bệnh nhân điều trị bằng bisphosphonates là hoại tử xương hàm, do đó không chỉ định can thiệp nha khoa trước khi điều trị bằng bisphosphonates vì nguy cơ hoại tử xương hàm .
Điều trị tràn dịch màng phổi ác tính:
Các phương pháp điều trị bao gồm: chọc hút dịch màng phổi, bơm hoá chất gây dính màng phổi qua catheter hoặc sonde dẫn lưu, bơm bột tacl hoặc trà sát màng phổi khi soi, mổ cắt màng phổi. Các phương pháp nói trên nên được cân nhắc áp dụng nếu liệu pháp hoá chất hoặc liệu pháp tia thất bại .
- Liệu pháp tia và hoá trị liệu:
Tràn dịch màng phổi ác tính do ung thư phổi tế bào nhỏ có thể đáp ứng tốt với hoá trị liệu ở một số ít bệnh nhân .
- Điều trị tại chỗ cục bộ: có hiệu quả giảm khó thở, giảm thời gian nằm viện, giảm chi phí và hạn chế biến chứng .
- Chọc hút dịch màng phổi: nhằm làm giảm khó thở và xác định mức độ tái phát của dịch. Nếu chọc hút dịch mà vẫn không giảm khó thở thì có thể do phổi không nở ra được hoặc do ung thư di căn bạch huyết toàn thân, huyết khối tĩnh mạch hoặc do xẹp phổi. Khó thở không giảm sau chọc hút dịch có thể do tai biến của kỹ thuật như tràn khí hoặc chảy máu màng phổi. Nếu dịch màng phổi nhiều lên sau khi chọc hút dịch thì nên chọc lại ngay để xác định có chảy máu màng phổi hay không. Những bệnh nhân nặng, thể trạng yếu, thời gian sống thêm dự kiến ít hơn 3 tháng thì nên chọc dịch điều trị. Tràn dịch màng phổi nhiều có đẩy trung thất sang bên đối diện thì hút nhiềudịch trong một lần có thể gây phù phổi cấp một bên. Nên theo dõi áp lực màng phổi trong quá trình hút dịch .
- Gây dính màng phổi: điều trị gây dính màng phổi chủ yếu cho những bệnh nhân không có chỉ định điều trị hoá chất toàn thân, không có tràn dịch dưỡng chấp hoặc xạ trị vào trung thất thất bại. Đây là biện pháp nhằm nâng cao chất lượng cuộc sống của bệnh nhân, kéo dài thời gian sống thêm. Các chất gây dính thường dùng là: bột talc, tetracyclin, bleomyxin, doxycylin, quinacrin .
Một nghiên cứu ở Anh (1966-1992) cho thấy tỷ lệ gây dính màng phổi thành công ở bệnh nhân tràn dịch màng phổi ác tính là 64%. Bột talc là tác nhân gây dính hiệu quả nhất (tỷ lệ thành công 93%); Corynebaclerium parvum: 76%, doxycyclin: 72%, bleomyxin: 54%. Tỷ lệ gây dính bằng bột talc, tetracyclin là 72%, với các thuốc chống ung thư như bleomycin, interferron-beta, cisplatin, 5FU, etoposid là 44% .
Một số nghiên cứu cho thấy hai phương pháp gây dính màng phổi bằng hỗn dịch bột talc qua đặt sonde màng phổi và dùng bột talc khô qua soi lồng ngực có tỷ lệ thành công giống nhau khi sử dụng tới 5g bột talc .
Tuy nhiên vẫn còn một số vấn đề tranh luận liên quan tới phương pháp gây dính màng phổi, ví dụ: cỡ sonde, thời gian lưu, tư thế bệnh nhân, thời gian nhỏ giọt thuốc và rút sonde .
Bột talc lần đầu tiên được sử dụng để gây dính màng phổi vào năm 1935, công thức hoá học là Mg4Si4010(OH)2. Bột talc được phun vào khoang màng phổi qua nội soi hoặc bơm vào màng phổi bột talc dạng hỗn dịch. Một nghiên cứu gần đây giữa bột talc dạng hỗn dịch (5g) với bleomyxin ( 60Units ) thấy 90% thành công sau hai tuần, nhóm dùng bleomyxin là79%. Một nghiên cứu so sánh giữa talc dạng bột và talc dạng hỗn dịch thấy rằng không có sự khác biệt về tỷ lệ thành công ở hai nhóm. Các tác giả cho rằng khi sử dụng bột talc ở dạng hỗn dịch thì nên xoay trở bệnh nhân trong vòng 1 giờ vì bột talc dạng hỗn dịch không thể phát tán hoàn toàn như là các thuốc hoà tan. Các số liệu thực nghiệm cho thấy các tế bào trung biểu mô bị tổn thương trong vòng mấy phút sau khi tiếp xúc với thuốc. Tổn thương tế bào trung biểu mô sẽ khởi đầu đáp ứng viêm dẫn tới xơ màng phổi, thời gian lưu sonde 1 giờ là đủ để hai bề mặt màng phổi trà xát vào nhau, thúc đẩy quá trình dính màng phổi .
Các tác dụng phụ của thuốc gây dính màng phổi thường gặp nhất là đau ngực và sốt. Tỷ lệ đau ngực từ 7-43%; sốt từ 10-59%. Sốt xuất hiện trong vòng 12 giờ đầu sau khi bơm bột talc và hết sau 48 giờ. Một số trường hợp có suy hô hấp cấp sau dính màng phổi trong tràn dịch màng phổi ác tính bằng cách bơm bột talc gây. Liều lượng bột talc từ 2-5g cho tỷ lệ thành công cao và biến chứng thấp .
Ngoài ra có thể cắt bỏ các nốt nhỏ ở phổi qua nội soi màng phổi sau khi định vị u trên chụp cắt lớp vi tính, đây là một phương pháp đáng tin cậy, ít biến chứng giúp không cần làm mở lồng ngực sinh thiết .
Theo Boutin C và cộng sự, gây dính bằng tetracyclin cho hiệu quả được 90% các trường hợp, nhưng sau 6 tháng có 50% số bệnh nhân bị tái phát .
Theo tổng kết của 16 tác giả trong 30 năm (1958-1986), gây dính bằng bột talc điều trị tràn dịch màng phổi ác tính đạt được hiệu quả 72-100%. Đặc biệt đạt kết quả rất tốt trong tràn dịch màng phổi do ung thư các loại khác nhau kể cả u trung biểu mô ác tính .
Gây dính màng phổi trong tràn dịch màng phổi ác tính do ung thư phổi đạt hiệu quả 96,7%; thời gian nằm điều trị trung bình của những bệnh nhân được gây dính là 1,26 tuần. Biến chứng hay gặp nhất sau soi màng phổi gây dính là đau tại chỗ 56,7%; tràn khí dưới da khu trú 16,7%; sốt nhẹ và vừa 20%, các biến chứng khác ít gặp như chảy máu ít, nhiễm trùng chân dẫn lưu đều không quá 6,7% .
- Biến chứng của soi màng phổi: soi màng phổi điều trị tràn dịch màng phổi ác tính là một thủ thuật an toàn, hiệu quả và ít biến chứng: biến chứng hay gặp nhất là đau tại chỗ 56,7%, tràn khí dưới da khu trú 16,7%, sốt nhẹ và vừa 20%, biến chứng khác ít gặp như chảy máu ít, nhiễm trùng chân dẫn lưu 6,7%. Không có biến chứng nặng như tử vong, suy hô hấp, phản ứng thuốc, mủ màng phổi trong và sau khi soi .
4. ĐIỀU TRỊ QUANG ĐÔNG (Photodynamic therapy)
Với sự xuất hiện của các dẫn xuất hematoporphyrin tiêm, điều trị các khối u ở đường thở bằng phương pháp quang đông của đã trở thành khả thi từ những năm 1970. Hiện nay, thường sử dụng hỗn hợp porphyrin, ví dụ: porfimer (photofrin) với liều chuẩn là 2 mg/kg tiêm tĩnh mạch chậm 5-10 phút. Thuốc được đào thải khỏi cơ thể trong vòng 72 giờ, nhưng được giữ lại lâu hơn trong mô khối u, mô da (30 ngày), gan, và lách. Do tồn tại lâu hơn trong các tế bào khối u và nội mạc mạch máu, phản ứng độc tế bào của porfimer có tính chọn lọc đối với tế bào khối u. Sau một thời gian nhất định (thường là 48 giờ), khối u được tiếp xúc với năng lượng ánh sáng, những tế bào chứa porphyrin sẽ xuất hiện phản ứng độc tế bào. Phản ứng này phụ thuộc chủ yếu vào quá trình oxy hóa, trong đó các phân tử oxy sẽ gây độc tế bào với sự hiện diện của ánh sáng kích thích. Các nội mạc mạch trong khối u đặc biệt dễ bị quang đông với sự tổn thương của mao mạch ngay sau khi điều trị .
Chỉ định:
- Ung thư phổi không chỉ định phẫu thuật cắt bỏ khối u được .
- Ung thư phổi tái phát sau phẫu thuật (tỷ lệ khoảng 10%) .
- Ung thư phổi có tổn thương đường thở ngoài phổi ở bệnh nhân không có chỉ định phẫu thuật và xạ trị .
- Điều trị tắc nghẽn và điều trị triệu chứng ở bệnh nhân ung thư phổi không tế bào nhỏ có tắc nghẽn đường thở một phần hoặc hoàn toàn .
Nguồn sáng:
Sự hấp thụ porfimer đạt cực đại ở bước sóng 405nm. Tuy nhiên, ánh sáng ở bước sóng đó gần như hoàn toàn bị hấp thụ tại bề mặt tế bào, do đó chỉ phá hủy tối thiểu phần ngoại vi khối u. Để quá trình phá hủy sâu hơn từ 5-10mm phải sử dụng ánh sáng bước sóng 630nm. Nguồn sáng thường dùng là bóng argon hoặc KTP (kali-titanyl-phosphate) phát laser lạnh. Ánh sáng được truyền qua hệ thống cáp quang, qua ống soi phế quản tới tổn thương. Sợi cáp quang thường có đầu hình trụ, có thể dẫn truyền ánh sáng theo chiều ngang 360 độ trong một vòng cung gần đầu sợi. Một thấu kính nhỏ có thể được sử dụng để tập trung ánh sáng theo một hướng về phía trước để điều trị các khối u nhỏ trên bề mặt. Đầu sợi quang này cũng khá cứng, cho phép đâm xuyên vào khối u nếu cần thiết. Thủ thuật được tiến hành khoảng 48 giờ sau khi tiêm nên chất porphyrin ở niêm mạc bình thường đã được đào thải gần như hết, do đó giảm thiểu thiệt hại cho các mô lành .
Tính liều quang đông:
Liều điều trị ban đầu thường là 200 Jun/cm2. Liều quang đông những lần điều trị sau phụ thuộc vào đánh giá tổn thương sau đó. Thông thường lần điều trị bổ sung tiến hành sau 2 ngày .
Tiến hành:
Nên siêu âm qua nội soi trước nếu có trang bị, thường sử dụng ống soi mềm. ống soi cứng chỉ nên sử dụng khi bệnh nhân không ổn định hoặc thiếu oxy hoặc dự kiến cuộc soi kéo dài. Gây tê tại chỗ tốt để loại bỏ hoàn toàn ho nhằm cố định dụng cụ phát quang dễ dàng và chính xác .
Đưa ống soi qua đường mũi thích hợp hơn khi trong thủ thuật quang đông. Khi ống soi tiếp cận tổn thương, áp sát thiết bị phát quang vào tổn thương nhằm bảo vệ niêm mạc bình thường khỏi tác động của ánh sáng và cung cấp nhiều năng lượng hơn để phá hủy khối u. Sau khi đạt liều điều trị, tắt nguồn sáng, hút chất hoại tử ra, rút soi phế quản. Tiến hành lần điều trị tiếp theo trong 48 giờ .
Biến chứng:
- Ho ra máu hay gặp sau thủ thuật. thường ho ra máu số lượng ít, tự hết .
- Đau ngực do phản ứng viêm .
- Khó thở, suy hô hấp cấp có thể xuất hiện trong vòng 24-48 giờ sau khi điều trị do phù nề, tăng tiết. Biến chứng này hay xuất hiện hơn khi tổn thương nằm ở khí quản hoặc với tiến hành với mức năng lượng cao, tổn thương tăng tiết, chất hoại tử nhiều khó hút ra hết. Biến chứng cũng có thể xảy ra sau khi điều trị tổn thương ở ngoại vi nếu chức năng phổi kém. Cần theo dõi sát, chỉ định thở máy kịp thời .
- Da nhạy cảm với ánh nắng mặt trời ngay sau khi tiêm porphyrin và kéo dài 4-6 tuần. Cần hướng dẫn cho bệnh nhân các biện pháp phòng ngừa nhạy sáng và nguy cơ cháy nắng. Bệnh nhân nên sử dụng quần áo bảo hộ và kính mắt khi tiếp xúc với ánh sáng mặt trời. Kem chống nắng không bảo vệ hiệu quả vì nó không lọc tất cả các bước sóng nhìn thấy được. ánh sáng mờ, ánh sáng từ nguồn sáng nhân tạo, nhất là từ tivi, không ảnh hưởng .
Hiệu quả:
Điều trị quang đông thường ứng dụng cho các khối u phổi không tế bào nhỏ nội phế quản giai đoạn đầu cũng như tắc nghẽn phế quản do ung thư. Quang đông còn được sử dụng để điều trị các tổn thương trong lòng đường thở, ung thư phế quản gốc tái phát, u tắc nghẽn phế quản ngoại vi, di căn của khối u ác tính, ho ra máu do dị dạng động tĩnh mạch nội phế quản .
Liệu pháp quang đông được các trung tâm sử dụng nhiều vì không tạo ra khói khi đốt và có thể được thực hiện trong một môi trường giàu oxy, tai biến thủng phế quản ít gặp hơn .
Liệu pháp quang đông có thể kết hợp thành công với các phương pháp điều trị khác như xạ trị áp sát và laser .
5 PHƯƠNG PHÁP CẮT LẠNH (Cryotherapy, cryoblation)
Cắt lạnh với nhiệt độ thấp là phương pháp phá huỷ mô một cách chọn lọc bằng cách làm lạnh các mô nhanh nhất có thể nhằm làm đông tế bào .
5.1.Cơ chế phá hủy mô, tế bào của phương pháp cắt lạnh
Phương pháp cắt lạnh làm tiêu hủy các mô, tế bào thông qua quá trình đóng băng mô, tế bào. Các tổn thương do đóng băng tế bào và mô xảy ra ở cấp phân tử. Quá trình phá hủy bị ảnh hưởng bởi nhiều yếu tố như tốc độ làm lạnh, tốc độ tan băng, nhiệt độ tối thiểu đạt được, hàm lượng nước của các tế bào, và số lượng chu kỳ đóng băng và tan băng .
Một số mô nhạy cảm với lạnh (da, niêm mạc, mô hạt), trong khi những mô khác chịu lạnh tốt hơn (mỡ, sụn, mô sợi, hoặc các mô liên kết). Tế bào khối u nhạy cảm với lạnh hơn nhiều so với tế bào bình thường .
- Rối loạn vi tuần hoàn ở mô bị làm lạnh: khi mô bị làm lạnh sẽ xuất hiện co thắt các động tĩnh mạch nhỏ và tổn thương nội mạc mạch, tăng tính thấm thành mạch, tăng độ nhớt máu, áp lực thủy tĩnh trong các vi mạch giảm, giảm lưu lượng máu. Những biến đổi trên dẫn đến kết dính tiểu cầu. Sự lưu thông dòng máu dừng lại nhanh chóng do huyết khối mạch. Các tổn thương mạch máu giải thích tác dụng cầm máu của phương pháp cắt lạnh không phải lúc nào cũng xuất hiện ngay lập tức .
- Trong những ngày sau liệu pháp lạnh: xuất hiện quá trình hoại tử tế bào do thiếu máu cục bộ .
- Quá trình phá hủy mô do phẫu thuật cắt lạnh mạnh hơn khi hóa trị hoặc xạ trị phối hợp
5.2 . Chất làm lạnh
Chỉ sử dụng chất làm lạnh ở dạng lỏng. Nhiệt độ cần thiết để làm cho hơn 90% tế bào chết là -200 đến -400C hoặc thấp hơn với tốc độ nhanh (-1000C/phút). Chất làm lạnh thường được sử dụng là nitơ lỏng, oxit nitơ và carbon dioxide .
- Nitơ lỏng có thể dễ dàng đạt được nhanh chóng nhiệt độ -1960C trong khoảng một phút
- Nitơ oxit (N2O) thường được sử dụng cho kỹ thuật cắt lạnh qua ống soi phế quản. Nó có thể tạo ra nhiệt độ -890C ở áp suất khí quyển .
- Carbon dioxide (CO2) cũng hay được sử dụng bởi vì nó đạt được nhiệt độ -790C. Carbon dioxide hay dùng cho phẫu thuật lạnh đối với tổn thương ngoài da. Tuy nhiên, nó không thích hợp để sử dụng cho phẫu thuật lạnh qua nội soi phế quản vì tạo tuyết ở áp suất khí quyển gây cản trở cho soi phế quản .
5.3. Phẫu thuật lạnh qua nội soi phế quản (còn gọi là áp lạnh qua nội soi)
Các thiết bị để phẫu thuật cắt lạnh đơn vị hiện đang được sản xuất tại Đức, Pháp, và Cộng hòa Séc; tuy nhiên FDA chỉ phê chuẩn các thiết bị của Đức .
Một thiết bị cắt lạnh có ba phần chính: giao diện điều khiển, dụng cụ áp lạnh và đường truyền kết nối giao diện điều khiển và xi lanh khí để thăm dò. Dụng cụ áp lạnh cứng hoặc nửa cứng chỉ có thể được sử dụng đối với ống soi phế quản cứng, dụng cụ áp lạnh mềm sử dụng đối với ống soi phế quản mềm. Đường kính của các kênh dụng cụ của ống soi mềm khoảng 2,6mm hoặc 3,2mm. Đối với dụng cụ áp lạnh cứng, giai đoạn tan băng xuất hiện ngay lập tức vì có một hệ thống hâm nóng. Đối với dụng cụ áp lạnh mềm, quá trình tan băng diễn ra tự phát và kéo dài .
Kỹ thuật :
Chuẩn bị:
- Xét nghiệm: Xquang ngực thường, CT-scans, xét nghiệm đông máu, khí máu và chức năng phổi .
- Ngừng liệu pháp chống đông cho bệnh nhân trước khi tiến hành kỹ thuật 24 giờ .
Tổn thương giống san hô phù hợp nhất với phương pháp áp lạnh. Đầu kim loại của dụng cụ áp lạnh (cryoprobe) được đặt trên bề mặt khối u hoặc đâm xuyên vào u để gây đông khối u tối đa. Ba chu kỳ đóng băng-tan băng được thực hiện ở mỗi vị trí. Các vị trí áp lạnh tiếp theo cách vị trí cũ 5-6mm. Qui trình này này tiếp tục cho đến khi xác định khối u đã được đông lạnh. Thể tích của vùng mô khối u bị đông lạnh trong một chu kỳ khi dùng nitơ lỏng lớn hơn so với nitơ oxit nên thời gian nội soi được rút ngắn .
Nếu có thiết bị đo điện trở, quá trình hâm nóng được bắt đầu khi điện trở đạt tới 250-500kilo-ohm. Chu kỳ đóng băng tiếp theo được bắt đầu khi điện trở giảm đến 50 kilo-ohm .
Khi dùng nitơ oxit thời gian đóng băng kéo dài khoảng 30 giây/chu kỳ. Không nên kéo dài thời gian này. Khi dùng nitơ lỏng thời gian đóng băng khoảng một phút/chu kỳ đóng băng đầu tiên, nhưng chu kỳ tiếp theo ngắn hơn .
Lần phẫu thuật lạnh tiếp theo tiến hành sau lần đầu 8-10 ngày sau. Ở lần tiếp theo: kiểm tra đánh giá phá hủy tổn thương, loại bỏ tổ chức hoại tử, áp lạnh lặp lại nếu cần thiết .
Biến chứng : Khó thở do phù nề: phù nề sau liệu pháp lạnh thường không nghiêm trọng, nên khó thở ít gặp hoặc nhẹ. Có thể dùng corticosteroid trong vòng 24 giờ sau liệu pháp lạnh đối với tổn thương khí quản hoặc dưới nắp thanh môn .
6. XẠ TRỊ ÁP SÁT (BRACHYTHERAPY)
Xạ trị áp sát là đưa nguồn xạ qua ống soi phế quản vào sát tổn thương ung thư nội phế quản để loại bỏ chúng. Nói cách khác, đây chính là chiếu xạ trong .
6.1. Kỹ thuật
Xạ trị áp sát trong ung thư phổi đòi hỏi phải đưa một nguồn xạ vào đường thở. Trước đây, nguồn năng lượng phóng xạ thấp được đưa qua ống soi phế quản cứng. Hiện nay chủ yếu sử dụng ống soi phế quản sợi mềm để đặt một ống polyethylene chứa nguồn xạ vào trong đường thở tiếp giáp với các khối u. Vị trí đặt nguồn xạ được xác định bằng chiếu và chụp Xquang ngực, sau đó qua catheter đưa nguồn xạ vào đường thở bằng tay hoặc bằng thiết bị điều khiển từ xa. Sử dụng bong bóng hoặc bao vỏ để làm cho catheter chứa nguồn xạ luôn cố định luôn ở vị trí trung tâm của đường thở và đảm bảo cho liều lượng chiếu đồng nhất. Tỷ lệ liều xạ phụ thuộc vào năng lượng và tốc độ phân rã của chất phóng xạ được sử dụng. Xạ trị áp sát liều thấp đòi hỏi thời gian tiến hành kéo dài 30-70 giờ và các biện pháp bảo vệ phóng xạ cồng kềnh. Xạ trị áp sát liều cao thường sử dụng iridi-192 cho phép giảm đáng kể thời gian điều trị, do đó có thể áp dụng cho bệnh nhân ngoại trú. Xạ trị áp sát liều cao đòi hỏi catheter phải rất cố định trong lòng đường thở, tiện lợi cho bệnh nhân, giảm chi phí điều trị. Nhiều cơ sở điều trị sử dụng phương tiện đưa nguồn xạ vào đường thở được điều khiển từ xa đã đơn giản hóa hoạt động bảo vệ bức xạ. Xạ trị áp sát liều cao thường được phân đoạn liều để tối ưu hóa hiệu quả và giảm tác dụng phụ. Thường thời gian điều trị không quá 1-2 tuần để giảm khó chịu cho bệnh nhân vì phải đặt ống soi nhiều lần .
6.2. Chỉ định
- Tắc nghẽn đường thở lớn do tổn thương ung thư nội khí phế quản .
- Điều trị bổ trợ cho những trường hợp sau phẫu thuật khối u ngoại vi hoặc ở bệnh nhân ung thư phổi giai đoạn đầu cắt phân thùy .
6.3. Chống chỉ định
- Có chẩn đoán mô bệnh là ung thư phổi không tế bào nhỏ hoặc di căn ung thư vào phổi .
- Bệnh nhân chống chỉ định điều trị laser YAG hoặc các phương pháp áp lạnh .
- Bệnh nhân chống chỉ định chiếu xạ ngoài vì chức năng phổi kém .
- Bệnh nhân khó thở, viêm phổi tắc nghẽn sau, ho ra máu, hoặc ho điều trị ít kết quả
- Có thể đưa catheter với nguồn xạ vào đúng vị trí cần thiết .
- Tiên lượng bệnh nhân có thể sống thêm trên 3 tháng .
Bệnh nhân ung thư phổi không phẫu thuật được hoặc ung thư tái phát hoặc di căn khối u ác tính vào đường hô hấp thường có chỉ định xạ trị áp sát. Chỉ nên điều trị cho các tổn thương nằm ở khí quản, phế quản gốc hoặc phế quản thùy dưới. Khối u có thể là bên ngoài hay trong đường thở hoặc là xâm nhiễm ung thư dưới niêm mạc, miễn là có thể đưa được ống thông chứa nguồn bức xạ vào đường thở .
6.4. Chống chỉ định
- Có rò phế quản .
- Tổn thương nội khí quản gây tắc nghẽn trung tâm nên được điều trị laser YAG và có thể stent trước, bởi vì ngay lập tức sử dụng xạ trị áp sát có thể gây phù nề mô và làm tắc nghẽn đường thở hoàn toàn .
- Không nên tiến hành xạ trị áp sát ở bệnh nhân không thể tiến hành nội soi phế quản và ở những bệnh nhân tiên lượng thời gian sống thêm quá ngắn .
6.5. Biến chứng
Biến chứng sớm:
- Gồm các biến chứng do soi phế quản và đặt catheter .
- Viêm phế quản và hẹp phế quản có thể xảy ra sau vài ngày hoặc một tuần sau khi điều trị với biểu hiện ho hoặc khó thở. Nguy cơ có biến chứng sớm ở những trường hợp ung thư tế bào lớn, điều trị laser trước, hoặc kết hợp với xạ trị đồng thời bên ngoài .
Biến chứng muộn có thể gặp với tỷ lệ 0 -42%, bao gồm:
- Ho ra máu nặng .
- Rò phế quản .
Để làm giảm biến chứng muộn cần đánh giá tổn thương động mạch, thành phế quản và trung thất bằng CT-scaner, cộng hưởng từ hay chụp động mạch trước khi xạ trị áp sát, đặc biệt khi điều trị thương tổn ở đường thở trung tâm .
6.6. Hiệu quả
Đối với tổn thương tắc nghẽn đường thở trung tâm: khoảng 70% bệnh nhân có cải thiện hơn 50% trong thời gian ít nhất sáu tháng. Các triệu chứng thuyên giảm rõ là ho ra máu, khó thở và ho .
Một số nghiên cứu kết hợp xạ trị áp sát với chiếu xạ ngoài cho thấy đã kéo dài thời gian sống thêm của bệnh nhân. Kết hợp xạ trị áp sát điều trị laser tại chỗ cho kết quả tốt hơn điều trị laser đơn thuần .