1. DCPX TRONG CHẨN ĐOÁN
Dược chất phóng xạ (DCPX) dùng trong chẩn đoán bệnh cần đáp ứng được những yêu cầu sau đây:
+ Loại bức xạ: DCPX lý tưởng dùng trong CĐ là chất phát tia gamma đơn thuần, do phân rã bắt điện tử hoặc do ổn định muộn (metastable). Các dược chất có lẫn alpha và beta sẽ không có lợi trong ghi hình vì những bức xạ này có khả năng ion hoá mạnh làm cho các mô bị tổn thương, mặc dù có thể có một số bức xạ xuyên qua được cơ thể nhưng không vào được các thiết bị ghi đo. Bức xạ alpha truyền năng lượng tuyến tính (LET) cao, gây tổn thương tế bào nhiều, không dùng trong chẩn đoán.
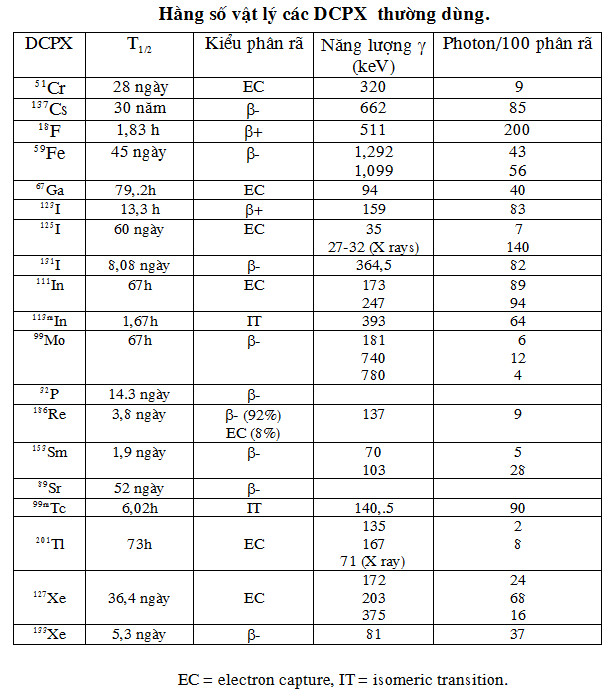
+ Năng lượng: để ghi hình tốt, chất phóng xạ lý tưởng phải có năng lượng bức xạ từ 100 keV đến 250keV, vì phù hợp với thiết kế hiện nay của các máy. Trên hoặc dưới giới hạn đó, chất lượng ghi hình sẽ kém đi. Mặc dù vậy, trên thực tế lâm sàng, có những chất có năng lượng cao hơn hoặc thấp hơn vẫn phải dùng, không thay thế được. 201Tl, 133Xe có năng lượng 70 đến 80 keV, 131I và 67Ga có năng lượng tương ứng 364 keV và 300 keV là những chất hay dùng trong chẩn đoán. Về mặt năng lượng thì những chất thích hợp hơn cả là 99mTc, 111In, 123I.
+ Tính khả dụng: DCPX cần có đời sống không quá ngắn để có thể vận chuyển thuận lợi từ nơi sản xuất tới nơi sử dụng, giá cả phải chăng, phù hợp với điều kiện kinh tế của bệnh nhân.
+ Phản ứng hoá học: 99mTc được coi là một DCPX tốt, dùng được cho nhiều loại xét nghiệm chẩn đoán khác nhau vì Tc có khả năng liên kết với nhiều hợp chất trong điều kiện sinh lý bình thường. Tc có thể tạo thành hợp chất với nhiều loại, từ các phân tử đơn giản như pyrophosphate tới các chất hữu cơ nhóm đường như glucoheptonate, từ peptide đến các kháng thể, từ các dạng colloide không hoà tan tới các kháng sinh và nhiều hợp chất khác nữa. Mặt khác việc dùng phóng xạ để đánh dấu cũng không đơn giản. Không phải chất phóng xạ nào cũng dùng được, không phải hợp chất nào cũng đánh dấu được.
+ Tỷ số đích - không đích: tỷ số đích - không đích cao mới tốt, nghĩa là DCPX phải vào nhiều ở nơi cần ghi hình ảnh so với các nơi khác trong cơ thể. Nếu tỷ số đích - không đích thấp hơn yêu cầu tối thiểu (tỷ số 5:1 là tối thiểu để ghi hình phẳng, 2:1 là tối thiểu để xạ hình cắt lớp SPECT) thì xạ hình sẽ không có giá trị chẩn đoán vì khó phân biệt giữa vùng bệnh lý và không bệnh lý. Ví dụ ghi hình tuyến giáp, đích là tuyến giáp, không đích là các mô khác ở cổ. Nếu tỷ lệ chỉ là 1,5:1 thì rất khó nhận dạng, ít nhất phải đạt 3:1. Khi tiến hành xạ hình xương sẽ có hai cặp đích và không đích. Đích và không đích thứ nhất là xương và phần mềm, giả thiết tỷ số xương: phần mềm là 5:1, đích thứ hai là ổ di căn và không đích là xương, giả thiết di căn/xương cũng là 5:1, thì tỷ số di căn/phần mềm sẽ là 25:1. Nếu tỷ số đích - không đích thấp thì cần làm xạ hình muộn (delayed), lúc đó đích còn tồn lưu phóng xạ và nơi không đích phóng xạ đã đào thải đi nhiều, hình ảnh sẽ rõ hơn. Nguyên nhân làm giảm tỷ số đích - không đích có nhiều: do loại dược chất phóng xạ không thích hợp, do kỹ thuật, do thiết bị...Đặc biệt phải chú ý nguyên nhân ở cơ thể người bệnh, ví dụ người bị bệnh tuyến giáp đang dùng các chất có nhiều nội tiết tố T3, T4 hoặc dùng các thuốc cản quang, phải chờ một thời gian cho hết thuốc mới ghi được hình tuyến giáp bằng 131I (tuyến giáp bị phong bế, chất phóng xạ không vào được).
+ Thời gian bán thải hiệu lực (effective half life): chất phóng xạ được coi là lý tưởng nếu thời gian bán thải hiệu lực =1,5 lần thời gian cần thiết để tiến hành một kỹ thuật chẩn đoán. Như vậy có thể đưa vào cơ thể một liều dược chất phóng xạ (DCPX) lớn để ghi hình tốt mà người bệnh lại bị một liều chiếu xạ nhẹ. Về toán học, có công thức như sau:
1/teff = 1/tbio + 1/tphys
Trường hợp tbio rất dài so với tphys (99mTc sulfur colloid trong gan) thì teff tương đương với tphys. Nếu tphys rất dài so với tbio thì teff = tbio (ví dụ: khí 133Xe trong phổi).
99mTc-MDP là chất có thời gian bán thải hiệu lực lý tưởng cho xạ hình xương, vì teff = 6h, trong khi đó quy trình xạ hình xương kéo dài 4h, vậy là đạt tỷ số 1,5: 1. Trong xạ hình gan, dùng 99mTc sulfur colloid, teff cũng là 6h nhưng quy trình xạ hình gan chỉ đòi hỏi 1h, như vậy tỷ số là 6:1. Tỷ số này không có nghĩa là hình ảnh ghi được không tốt mà chỉ là thời gian chất phóng xạ lưu lại trong gan dài, không có lợi cho bệnh nhân. Nếu dùng Tc- macroaggregate, với teff = 3h thì tỷ số sẽ là 3: 1, liều chiếu xạ trong cơ thể bệnh nhân sẽ giảm được 50%.
+ An toàn cho người bệnh: các DCPX đưa vào cơ thể phải đảm bảo an toàn, không độc hại với người bệnh. Tuy nhiên, trên thực tế có một số chất biết là có độc mà vẫn phải dùng. Ví dụ: ion Tl là chất độc với tim (cardiotoxic) nhưng hiện nay còn dùng trong chẩn đoán bệnh tim. Lý do: lượng Tl đưa vào không nhiều, với liều dùng 3 mCi chỉ tương đương 42ng Tl, cơ thể có thể chấp nhận được (không kể trường hợp quá mẫn cảm).
Để đảm bảo an toàn cho người bệnh và cho cán bộ chuyên môn, cần tuân thủ nguyên tắc ALARA (as low as reasonably achievable). Liều dùng cho bệnh nhân càng nhỏ càng tốt (nhưng phải ghi được hình ảnh rõ), với trẻ em phải giảm liều, phải nhớ rằng ghi hình cắt lớp (SPECT) đòi hỏi liều xạ cao hơn ghi hình phẳng (planar imaging).
2. ĐẶC TÍNH CỦA DCPX DÙNG TRONG ĐIỀU TRỊ
+ Loại bức xạ: trong điều trị cần những loại bức xạ có quãng đường đi ngắn và có độ truyền năng lượng tuyến tính (LET) cao để hủy diệt tế bào tại chỗ rất tốt mà không ảnh hưởng tới các mô lân cận. Chất phát bức xạ beta đáp ứng được những yêu cầu này hơn các chất phát ra gamma. Các chất phát ra alpha cũng có khả năng phá hủy tế bào mạnh nhưng rất khó sử dụng trong thực tế. 131I là chất được dùng nhiều trong điều trị bệnh cường giáp, bệnh ung thư tuyến giáp. 131I phát ra gamma và beta, gamma giúp cho ghi hình và đo độ tập trung để chẩn đoán bệnh, beta có tác dụng điều trị. Tác dụng hủy diệt tế bào tuyến giáp của 131I 90% do tia beta, chỉ có 10% là do tia gamma.
+ Năng lượng: mục tiêu của điều trị là hủy diệt tế bào, vì vậy cần dùng các chất có năng lượng cao. Những chất phát bức xạ beta với mức năng lượng từ 1 MeV trở lên là thích hợp. Nếu đồng thời phát bức xạ gamma sẽ có lợi cho việc ghi hình trong quá trình điều trị (trường hợp 131I).
+ Thời gian bán thải hiệu lực: thời gian ngắn quá, hiệu quả điều trị sẽ thấp, thời gian dài quá sẽ có hại cho cơ thể. Thời gian hiệu lực của DCPX trong điều trị thông thường tính bằng ngày hoặc giờ. Để điều trị bệnh tuyến giáp thì 131I là chất có teff = 6 ngày rất thích hợp, chất Holmium-166 ferric hydroxide macroaggregate (FHMA) có teff = 1,2h dùng để tiêm vào bao hoạt dịch của khớp xương, rất phù hợp với yêu cầu điều trị.
+ Tỷ số đích- không đích: trong chẩn đoán, tỷ số này có ý nghĩa quan trọng, nhưng trong điều trị, tỷ số này còn quan trọng hơn nữa và có ý nghĩa quyết định. Ví dụ: điều trị di căn ung thư vào xương, DCPX phải tập trung nhiều ở ổ di căn để không ảnh hưởng xấu tới xương, tủy và phần mềm. Yêu cầu DCPX phải tinh khiết về mặt hoá học và tính toán đo lường chính xác lượng đưa vào.
+ An toàn bức xạ: cần chú ý tới việc bảo đảm an toàn cho bệnh nhân và cho cán bộ nhân viên. Phải luôn chú ý tới 3 yếu tố: thời gian (T), khoảng cách (K) và che chắn. Khi cho bệnh nhân dùng thuốc, khi chăm sóc bệnh nhân, cán bộ nhân viên cần thành thạo công việc, làm nhanh gọn để thời gian tiếp xúc với nguồn xạ ngắn nhất, người nhà và nhân viên chăm sóc không được quá gần người bệnh, khi cần tiêm hoặc lấy máu bệnh nhân làm xét nghiệm phải dùng ống tiêm có bọc chì. Theo quy định của quốc tế và chính thức áp dụng ở nước ta, nếu người bệnh dùng một liều < 30 mCi thì được phép ngoại trú, trường hợp dùng liều cao hơn (50, 100 mCi hoặc hơn nữa) thì người bệnh cần nằm ở bệnh viện cho tới khi đo ở cách vùng ngực bệnh nhân 1m, suất liều đạt < 5 mR/h thì được phép ra viện.
+ Tính kinh tế và tính khả dụng: DCPX phải đạt được yêu cầu dễ sử dụng, ít độc hại và giá thành không cao, nếu không thoả mãn những yêu cầu đó thì không thể ứng dụng rộng rãi được.
+ Đặc tính của những DCPX dùng đường tiêm: những dược chất phóng xạ dùng đường tiêm phải đạt hai yêu cầu: vô khuẩn và không chí nhiệt tố. Chí nhiệt tố là những hợp chất hoà tan trong nước, không bị phá hủy ở nhiệt độ của nồi hấp (autoclave), thấm qua được màng lọc, gây sốt khi tiêm vào cơ thể người và động vật. Đó thường là các nội độc tố của trực khuẩn. Ngoài hai yêu cầu trên, còn phải chú ý tới độ đẳng trương của dung dịch tiêm (tương đương dung dịch NaCl 0,9%) và độ pH tương tự máu (pH = 7,5). Nếu phải dùng dung dịch ưu trương hoặc nhược trương để tiêm tĩnh mạch thì phải tiêm chậm.
Cần đảm bảo DCPX đưa vào đúng liều lượng, vì vậy phải đo trên máy chuẩn liều. Sai số về liều lượng cho phép là ± 10%.
3. DƯỢC CHẤT PHÓNG XẠ DÙNG TRONG Y HỌC HẠT NHÂN
Những DCPX dùng trong YHHN đều là nhân tạo, được tạo ra từ các bình sinh xạ (generator), từ lò phản ứng hạt nhân (nuclear reactor) hoặc từ các máy gia tốc vòng (cyclotron).
+ Phân nhóm: có thể chia các DCPX thành bốn nhóm chính.
- Nhóm 1: Gồm các chất phát ra positron, ví dụ: 11C, 13N, 15O, 18F. Các chất này đều được tạo ra từ máy gia tốc vòng. Thường là sản xuất ra dùng ngay tại chỗ, không vận chuyển được vì T1/2 rất ngắn (15O: 2 phút, 11C: 20,4 phút, 13N: 10 phút, chỉ có 18F lâu hơn cả: T1/2 = 1,82h). Nơi sản xuất chịu trách nhiệm về chất lượng của các DCPX đó, không có cơ quan nào kiểm tra, cấp phép vì không đủ thời gian để làm các thủ tục.
- Nhóm 2: Những chất do máy gia tốc vòng tạo ra nhưng phát bức xạ gamma như: 67Ga, 201Tl, 123I, 111In...Những chất này có đời sống tương đối dài hơn nhóm 1, nên phần lớn (trừ 123I) có thể vận chuyển đi xa được và có thể xuất nhập khẩu qua các quốc gia (67Ga = 79,2h, 111In = 67h, 201Tl = 73h). Đặc biệt, chất 201Tl dùng trong ghi hình là nhờ bức xạ X đặc tính của 201Hg, vì bức xạ gamma (135 và 167keV) chiếm tỷ lệ quá ít.
- Nhóm 3: Những chất được tạo ra từ bình sinh xạ, như 99mTc, 113mIn. Chất được dùng nhiều nhất là 99mTc vì mấy lý do: mức năng lượng phù hợp với yêu cầu của thiết bị ghi hình hiện đại (140 keV), thời gian T1/2 vừa phải (6h) và dễ gắn vào các chất để đưa vào cơ thể mà không ảnh hưởng tới hoạt động chức năng sinh lý của các cơ quan. Có tới 85% các ghi hình trong YHHN ở các nước tiền tiến được thực hiện với 99mTc.
- Nhóm 4: Những chất là sản phẩm phụ của sự phân rã 235U từ lò phản ứng hạt nhân. Sau khi tinh chế chúng ta thu được một số DCPX quan trọng và được dùng nhiều như 131 I, 133 Xe.
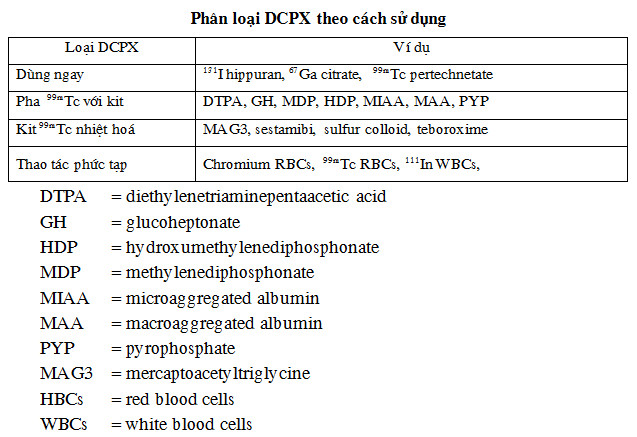
+ Phân loại theo cách sử dụng :
Các DCPX còn có thể được xếp loại theo cách sử dụng:
- DCPX dùng được ngay không phải xử lý kỹ thuật gì khác.
- DCPX phải pha chế với các kit.
- DCPX pha chế với kit và đun nóng.
- DCPX pha chế với những thao tác kỹ thuật không đơn giản.
+ Pha chế DCPX:
Phần lớn DCPX được đưa vào cơ thể bằng đường tiêm tĩnh mạch, vì vậy phải tuân thủ quy tắc vô trùng. Phải chú ý lau cồn sạch sẽ nút lọ trước khi đưa kim tiêm vào. Không để lọt không khí vào trong lọ, vì chỉ cần hàm lượng ôxy của 0,1 ml không khí cũng đủ để phá hủy hoàn toàn ion thiếc của kit đưa vào (trong thao tác gắn 99mTc vào hồng cầu). Không khí trong phòng cũng không phải là vô trùng, bởi vậy nếu bơm không khí vào để đẩy thuốc ra cho dễ cũng có thể làm ô nhiễm DCPX.
Khi lấy dung dịch pertechnetate cần lấy ngay vào dung dịch nước muối sinh lý, nếu lấy pertechnetate ra một lúc sau mới hoà vào nước muối sinh lý thì có thể làm cho một số liên kết bị tách ra và trong dung dịch sẽ có nhiều Tc dưới dạng tự do.
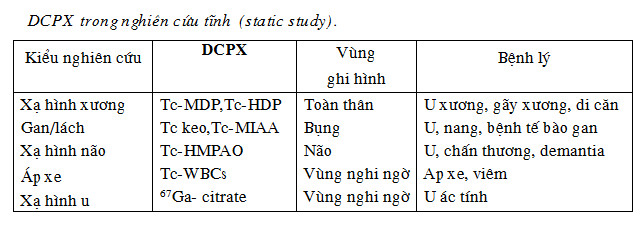
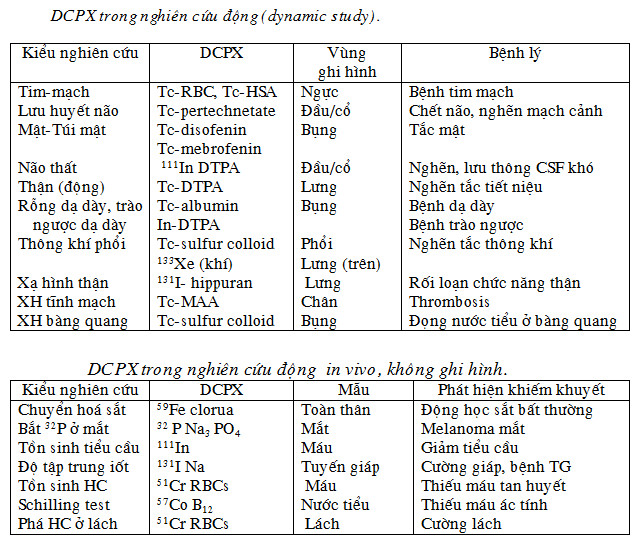
4. Các phương pháp chế tạo hạt nhân phóng xạ
Hầu hết các hạt nhân phóng xạ tự nhiên đã được tìm thấy. Các hạt nhân này thường có đời sống quá dài nên không thích hợp cho sử dụng trong y học hạt nhân. Các hạt nhân phóng xạ sử dụng trong y học phải có thời gian bán huỷ vật lý đủ ngắn, năng lượng vừa phải để tránh liều hấp thụ không có lợi cho bệnh nhân. Những hạt nhân này đều được sản xuất bằng phương pháp nhân tạo.
4.1. Hệ thống sinh phóng xạ (generator)
Một trong những vấn đề thực tế trong y học hạt nhân phải đối mặt đó là việc tìm kiếm các hạt nhân phóng xạ hay ĐVPX lý tưởng là phải có thời gian bán rã ngắn (có thể tính theo giờ, ngày hoặc tuần). Nhưng những ĐVPX này cũng phải đáp ứng đủ điều kiện về thời gian vận chuyển từ các trung tâm sản xuất đến các đơn vị sử dụng và các khoa y học hạt nhân. Một phương pháp hữu hiệu để giải quyết tình trạng này đó là việc sử dụng các hệ thống máy phát hạt nhân phóng xạ. Các hệ thống này thường chứa đựng 1 đồng vị mẹ với thời gian bán rã dài và một đồng vị con với thời gian bán rã ngắn.
Hệ thống máy phát và thời gian bán rã của đồng vị mẹ và đồng vị con
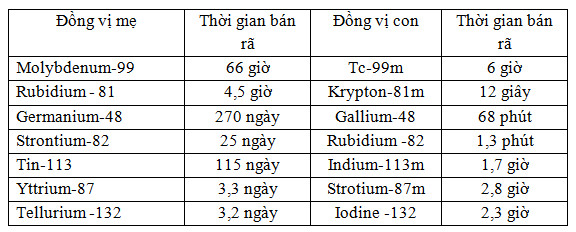
Máy phát có thể được vận chuyển từ nơi cung cấp đến các trung tâm ứng dụng lâm sàng mà thời gian bán rã của hạt nhân phóng xạ hay ĐVPX con vẫn phù hợp cho chẩn đoán lâm sàng. Trong những năm qua có rất nhiều hệ thống máy phát được khám phá.
Vấn đề tách đồng vị con ra khỏi đồng vị mẹ trong các hệ Generator thường đơn giản. Cách tách chiết dựa vào trạng thái hoá trị khác nhau của đồng vị con và mẹ. Thông thường, các Generator được cấu tạo bằng cột sắc ký, trong đó, hạt nhân mẹ được hấp thụ lên một số chất giá như Resin, nhôm hoặc các chất trao đổi ion khác. Hạt nhân con có hoá trị khác với mẹ nên có ái lực hóa học yếu hơn hạt nhân mẹ đối với chất giá, do đó có thể dùng dịch chiết thích hợp để chiết ra khỏi cột sắc ký.
Hệ Generator thường dùng trong bệnh viện là: 99Mo/99mTc, 113Sn/113mIn, 68Ge/68Ga, 83Y/87Sm, 82Sr/82Rb...Generator 99Mo/99mTc là những loại được dùng nhiều nhất trong các khoa Y học hạt nhân. Sau đây là nội dung chi tiết về loại Generator này.
- Những tính chất cơ bản của một hệ thống sinh phóng xạ:
. Hạt nhân con sinh ra với độ tinh khiết hoá phóng xạ và tinh khiết hạt nhân phóng xạ cao.
. Phải an toàn, đơn giản trong thao tác.
. Vô khuẩn, không có pyrogen.
. Khả năng tách chiết dễ, đa dạng.
. Đời sống hạt nhân phóng xạ con phải ngắn hơn 24 giờ.
Hệ thống Generator vững chắc để điều chế 99mTc bao gồm 2 cột sắc ký bằng oxit nhôm vô khuẩn. Cột thứ nhất cho molybden hấp phụ lên. Cột thứ 2 để tinh khiết lại, đề phòng Mo bị tách ra nhiều. Cột này nhằm tăng độ tinh khiết cho 99mTc nên có thêm một bộ phận lọc khí vào. Do cấu trúc như vậy mà loại này đảm bảo vô khuẩn, không có chất gây shock, gây sốt và an toàn phóng xạ. Generator này theo nguyên lý khô, do đó quá trình phân huỷ do phóng xạ (radiolyse) giảm xuống nhiều. Thể tích chiết mỗi lần 5ml, trong dung dịch chiết không có chất oxy hoá.
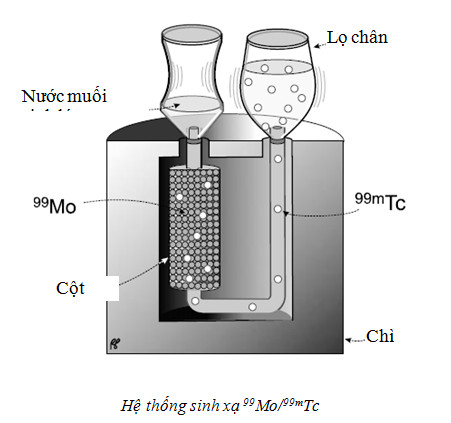
Để bảo đảm vệ sinh các đầu kim của Generator và tránh nhiễm bẩn, ở các đầu kim đều phải có nắp đậy, khi chiết phải tiến hành các bước như sau:
+ Thay nắp đậy ở 2 đầu kim bằng 2 lọ thủy tinh nhỏ (như lọ penixillin) chân không (lọ này cho vào container chì để bảo vệ bức xạ).
+ Sau khi chiết xong, lấy lọ có chứa 99mTcO4 ra và thay vào một lọ chân không mới để bảo vệ vô khuẩn.
+ Lưu 2 lọ thủy tinh trên cho đến lần chiết sau.
Hoạt tính cho trước của Generator 99mTc là cơ sở để tính hoạt tính cho những lần chiết với chu kỳ chiết là 23 giờ. Hoạt tính của mỗi lần chiết ở những thời điểm khác nhau được tính theo bảng dựa vào các hệ số tính sẵn.
- Các thông số chất lượng:
Mặc dù hệ thống máy phát được kiểm soát chất lượng rất nghiêm ngặt trước mỗi lần lô hàng được xuất. Nhưng việc kiểm tra chất lượng của dung dịch chiết mỗi lần tách chiết vẫn rất quan trọng. Các bước kiểm soát chất lượng là thể hiện tốt thực hành y tế (GMP) và cần thiết để đáp ứng các quy định và các hướng dẫn khác nhau của chính phủ và các tổ chức y tế. Dịch chiết từ Generator cho mỗi lần là 5 ml dung môi NaCl 0,9%, bảo đảm vô khuẩn với nồng độ hoạt tính cao.
+ Độ tinh khiết hóa chất:
Cần kiểm tra trong sản phẩm dung dịch chiết sự hiện diện của chất Al2O3 rò từ cột nhôm chứa 99Mo. Thành phần Al+3 dưới 2 mg/ml. Lượng nhôm quá nhiều sẽ làm ảnh hưởng đến khả năng phân bố sinh lý của một số dược chất phóng xạ ví dụ như 99mTc-Sulfur colloid (tăng hấp thu ở phổi) và 99mTc-MDP (tăng hấp thu ở gan).
+ Tinh khiết hoá phóng xạ: Hóa trị của 99mTc trong dung dịch chiết từ máy phát là +7 và ở trong hợp chất pertechnetate (TcO4-2). Trong lâm sàng natri pertechnetate được sử dụng như một DCPX và dùng gắn nhãn với dược chất có sẵn trên thị trường, hóa trị của nó trong trạng thái oxy hóa +7. Theo dược điển Mỹ (USP) thì dung dịch chiết của 99mTc phải có hoạt độ đến 95% hoặc hơn và có hóa trị +7.
+ Độ tinh khiết hạt nhân phóng xạ:
Trong dung dịch chiết từ Generator 99Mo/99mTc hạt nhân phóng xạ mong muốn duy nhất đó là 99mTc. Tất cả các hạt nhân phóng xạ khác đều coi là chất tạp và đều không mong muốn, bởi vì nó sẽ mang đến bức xạ không cần thiết cho bệnh nhân và cũng không mang lại lợi ích lâm sàng.
Tạp chất phóng xạ phổ biến nhất trong dung dịch chiết chính là đồng vị mẹ, 99Mo. 99Tc là đồng vị con của 99mTc qua quá trình đồng phân chuyển tiếp cũng được tìm thấy nhưng không được coi là tạp chất của hạt nhân phóng xạ. Mặc dù 99Tc có thể là một vấn đề trong quá trình gắn với chất mang nếu nhìn từ góc độ hóa học, tuy nhiên từ góc độ an toàn bức xạ cũng như y tế đó không phải là vấn đề và không dùng để kiểm tra tạp chất của hạt nhân phóng xạ. Thời gian bán rã của 99Tc là 2,1 x 105 năm. Nó tạo đồng vị con ruthenium-99 ổn định từ quá trình bán rã.
Giới hạn hoạt độ của 99Mo trong dung dịch chiết được cho phép bởi Ủy Ban Pháp Quy Hạt Nhân (Nuclear Regularory Commission -NRC) và phải được kiểm tra mỗi lần chiết tách. Theo giới hạn cho phép của NRC, hoạt độ của 99Mo không quá 0,15 mCi trong 1mCi hoạt độ của 99mTc trong liền tiêm. Bởi vì thời gian bán rã của 99Mo dài hơn so với thời gian bán rã của 99mTc nên tỉ lệ này tăng dần theo thời gian.
+ Độ pH từ 4 ¸ 7
- Đánh dấu 99mTc vào in vivo kit
99mTc đứng với Mangan và Rhenium trong nhóm phụ của cột VII, do đó nó có thể có nhiều mức oxy hoá khác nhau, có thể tồn tại với các hợp chất từ hóa trị 7+ đến 1-, tại hoá trị 7+ ở dạng pertechnetat trong Generator là dạng bền nhất. Những hợp chất sử dụng trong y học hạt nhân với 99mTc không phải ở dạng pertechnetat mà ở dạng bị khử để gắn với các chất tạo nên những liên kết bền. Các hợp chất đánh dấu với 99mTc có các loại liên kết chelat, keo (protein đông vón) và các dạng hạt.
Hợp chất Na99mTcO4 ở dạng dung dịch muối vô cơ được chiết trực tiếp từ Generator 99Mo/99mTc. Ngay từ những ngày mới phát triển YHHN, dạng này được dùng tiêm tĩnh mạch, ghi hình tĩnh bằng scanner để xác định hình thái và chức năng tuyến giáp, tuyến nước bọt, dạ dày. Đặc biệt để ghi hình não phát hiện khối u hay ứ trệ tuần hoàn nặng. Na99mTcO4 là chất đặc hiệu và lý tưởng để ghi hình não với scanner và Gamma camera và vẫn chưa có chất nào thay thế. Nó có những ưu điểm sau đây:
+ Có chu kỳ bán huỷ vật lý và mức năng lượng photon vừa đủ cao (143 keV), thích hợp cho ghi đo bằng in vivo.
+ Có thể dùng tới 30 mCi nhưng liều bức xạ cho bệnh nhân lại tối thiểu.
+ Hợp chất này không có chất mang nên không có độc chất hoá học.
+ Tỷ số não trên máu đạt cực đại sau khi tiêm khoảng 30 ¸ 60 phút. Có thể xác định được hình dáng, vị trí, độ lớn và bản chất thương tổn của não.
Dung dịch Na99mTcO4 còn được dùng để đánh dấu vào các in vivo kit thường nhập kèm với Generator theo yêu cầu. Na99mTcO4 rất dễ liên kết chelate với các hợp chất trong kit để tạo thành thuốc phóng xạ dùng ngay trong YHHN.
4.2. Chế tạo từ lò phản ứng hạt nhân
Từ lò phản ứng có 2 cách chế tạo hạt nhân phóng xạ: tinh chế từ sản phẩm do phân hạch hạt nhân và điều chế bằng phương pháp bắn phá hạt nhân bia.
- Tinh chế từ sản phẩm do phân hạch hạt nhân: Trong lò phản ứng hạt nhân có chứa những thanh nhiên liệu phân hạch, thường là 238U và 235U. Trong quá trình phân hạch sẽ tạo ra nhiều hạt nhân phóng xạ khác nhau. Những sản phẩm do phân hạch còn được gọi là “tro” của lò phản ứng. Có thể tinh chế từ tro phóng xạ để thu được một số hạt nhân phóng xạ cần dùng trong YHHN như 90Sr, 99Mo, 131I... Điều chế hạt nhân phóng xạ theo phương pháp này có hạn chế là hiệu suất thấp và không đáp ứng đủ loại nhân phóng xạ theo yêu cầu.
- Điều chế bằng phương pháp bắn phá hạt nhân bia: Lò phản ứng bao giờ cũng có một số lượng lớn neutron. Neutron sinh ra có năng lượng rất lớn, tốc độ rất nhanh. Phải dùng các thanh điều khiển làm chậm tốc độ của neutron thành neutron nhiệt. Những neutron nhiệt này được ứng dụng vào mục đích bắn phá các hạt nhân bền (bia) tạo ra các hạt nhân phóng xạ mới, vì vậy các nhân phóng xạ được tạo ra theo cách này thường có dư neutron (phân rã beta âm). Đại đa số các nhân phóng xạ thường dùng trong YHHN được chế từ lò phản ứng. Một số hạt nhân phóng xạ thông dụng dùng trong YHHN như sau:
Một số hạt nhân phóng xạ từ lò phản ứng:
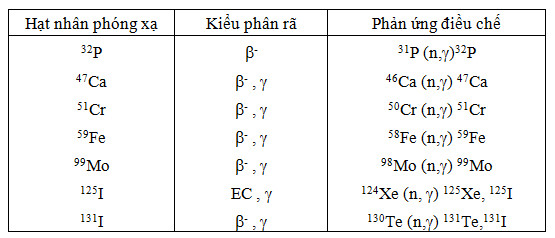
Nhược điểm của việc sản xuất ĐVPX từ lò phản ứng là về mặt hóa học ĐVPX và nguyên tố đích giống nhau, rất khó tách. Nghĩa là các ĐVPX sản xuất theo phương pháp này không phải là carrier-free.
+ Iod phóng xạ:
131I dưới dạng iodide natri là thuốc phóng xạ quan trọng đầu tiên trong y học hạt nhân lâm sàng. Nó được sử dụng dành riêng cho các nghiên cứu của tuyến giáp trong những năm cuối thập niên 40 của thế kỷ trước. Sau đó 131I đã được sử dụng như là chất đánh dấu cho nhiều dược chất phóng xạ, bao gồm cả huyết thanh albumin, macroaggregated albumin, và một số kháng thể, cũng như chụp xạ hình thận (hippuran), chụp xạ hình thượng thận (metaiodobenzylguanidine) và đánh dấu cho các chất dẫn xuất cholesterol.
Nhược điểm của 131I gồm năng lượng photon cao (364 keV), thời gian bán rã dài (8 ngày), và có phân rã tia beta kèm theo.
131I đóng vai trò quan trọng trong y học hạt nhân với các ứng dụng trong lâm sàng như điều trị cường giáp và ung thư tuyến giáp, sử dụng cho một số ứng dụng trong chẩn đoán như đánh dấu kháng thể và đánh dấu các tác nhân tuyến thượng thận.
Việc kiểm soát chất lượng DCPX gắn 131I là rất quan trọng vì nó sẽ giúp giảm sự phơi nhiễm bức xạ không cần thiết đối với tuyến giáp. Nếu điều kiện cho phép nên dùng 123I thay thế cho 131I vì 123I có thời gian bán rã ngắn hơn và năng lượng photon 159 keV sẽ phù hợp hơn trong ghi hình trên máy Gamma camera. Hạn chế của việc sử dụng 123I là chi phí tương đối cao và chu kỳ bán rã ngắn (13giờ).
+ Indium -111:
Một chất đánh dấu đa năng trong một loạt các ứng dụng của y học hạt nhân lâm sàng là 111In. Năng lượng photon từ 172 keV tới 245 keV, thuận lợi hơn so với 131I. Thời gian bân rê lă 2,8 ngày cho phép xạ hình liên tục trong nhiều ngày, thường được sử dụng trong đánh giá bệnh viêm (111In được gắn với bạch cầu) và xạ hình với các kháng thể. 111In- pentetreotide là một hợp chất có chứa chuỗi axit amin nhằm liên kết với thụ thể nội tiết somatostatin tìm thấy trong các khối u gốc thần kinh nội tiết.
+ Thalium -201:
201Tl được ứng dụng trong lâm sàng vào đầu những năm 1970 trong xạ hình tưới máu cơ tim. Tl có tác dụng tương tự như K, với sự thanh thải qua lớp đệm mao mạch cơ tim cao (85%). Do đó Tl có thể dùng để ghi hình đánh giá lượng máu chảy đến vùng cơ tim có khả năng sống. Năng lượng của các tia gamma là 135 keV và 167 keV.
4.2.3. Chế tạo từ máy gia tốc vòng
Các máy gia tốc hạt tích điện được chia thành hai nhóm dựa trên phương pháp gia tốc, đó là gia tốc thẳng và gia tốc vòng. Gia tốc hạt trong cả 2 nhóm được thực hiện do lực hút tĩnh điện giữa các hạt tích điện và ống tích điện trái dấu được ngăn cách nhau bằng bộ phận cách điện.
Máy gia tốc vòng có cấu tạo hình xoắn ốc. Các đoạn ống vòng chứa các đĩa hình bán nguyệt, tích điện trái dấu. Các hạt tích điện cần tăng tốc đi qua mỗi đĩa cực này lại được tăng tốc một lần, kết quả có được các hạt với năng lượng rất lớn, có thể bắn các hạt năng lượng lớn (proton, deutron hoặc hạt alpha) vào trong nhân và vì vậy sẽ tạo được những nhân có dư proton, các chất phân rã beta dương hoặc bắt điện tử.
Ví dụ: 127I khi được bắn phá bởi một proton năng lượng 60MeV, 5 neutron được phát ra và 127I chuyển thành 123Xe, sau đó qua phân rã beta dương và bắt điện tử chuyển thành 123I, dùng để ghi hình rất tốt trên máy SPECT. Phương trình diễn biến như sau: 127I (p,5n) 123Xe ® 123 I
Hoặc đối với 67Ga: 68Zn (p, 2n) 67Ga.
Các hạt nhân sản xuất từ gia tốc vòng thường không có chất mang vì hầu hết là phản ứng (p,n) và (d,n).Vì vậy nguyên liệu đích và sản phẩm phóng xạ không có cùng tính chất hóa học. Các loại máy gia tốc vòng có công suất dưới 30 MeV thì thường sản xuất được các hạt nhân phóng xạ là 18F, 11C, 15O, 13N, 124I, 123I. Máy có công suất trên 30 MeV thì sản phẩm thường là 201Tl, 18F, 11C, 15O, 13N, 124I, 123I.
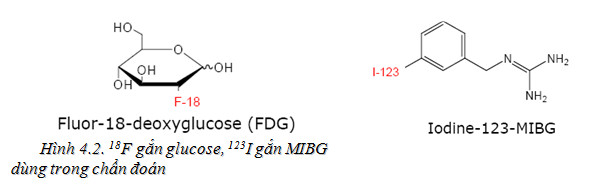
Hiện nay kỹ thuật ghi hình PET, đặc biệt là PET/CT đang được ứng dụng rộng rãi trong ghi hình chẩn đoán và theo dõi điều trị ung thư, tim mạch, thần kinh... Thuốc phóng xạ dùng cho PET đã và đang có giá trị ngày càng to lớn cùng với sự phát triển của kỹ thuật PET trong y học hạt nhân. Dưới đây giới thiệu một số nội dung sản xuất thuốc phóng xạ phục vụ cho PET. Số lượng các loại hạt nhân phóng xạ phát positron như 11C, 13N, 15O và 18F là rất lớn trong các hợp chất hữu cơ. Thời gian bán huỷ vật lý của hầu hết các hạt nhân này là tương đối ngắn (nhỏ hơn 2 giờ) và hoạt độ riêng (specific activity: SA) theo lý thuyết là rất cao.
Tiến bộ lớn nhất của PET là có khả năng ghi hình và nghiên cứu các quá trình hóa sinh in vivo mà không gây tác động hoặc biến đổi đến nội môi trong cơ thể bệnh nhân. Các nguyên tố có nguyên tử số thấp như carbon, nitrogen, oxygen và phospho là bền vững trong tự nhiên.Việc phát triển máy gia tốc từ năm1930 đã tạo ra cơ hội sản xuất các đồng vị phóng xạ phát positron của carbon (11C), nitrogen (13N) và oxygen (15O).
- Sản xuất 11C:
Phản ứng thông thường nhất để sản xuất 11C là bắn phá bằng chùm proton vào nguyên tử 14N dạng tự nhiên dưới dạng bia khí N2 (Schlyer 2003). Vì N2 là khí trơ không làm nhiễu tính chất hóa học của carbon và có thể dễ bị loại ra. Bằng cách trộn một lượng nhỏ (< 1%) oxy hoặc hydro vào khí N2 bia, sẽ có dạng hóa học của 11C được sản xuất trong bia có thể là CO2[11C] hoặc là CH4[11C]. Lọ đựng bia dạng khí được làm từ ống nhôm tròn (hoặc hình nón) và có thể nạp khí vào (10 ¸ 100 ml) dưới áp suất 300 ¸ 800 pascal. Cường độ chùm tia là từ 20 ¸40 mA. Điều quan trọng là cần chuẩn bị hoặc đánh bóng bên trong lọ bia bằng nhôm để giảm đáng kể nhiễm tạp carbon tự nhiên. Vì khí N2 tự nhiên cũng có tạp chất là khí CO2, nên đặc biệt phải dùng dạng tinh khiết cao (99,99999%) để làm hạt nhân bia. CO2[11C] có thể được sản xuất trong hầu hết các bia của máy gia tốc thông thường với SA = 5 ¸ 20 Ci/mmol tại EOB. Ngay cả khi cần SA cao hơn cũng có thể bắn phá và thu được CH4[11C] trực tiếp trong bia.
- Sản xuất 13N:
Vì 13N có T1/2 rất ngắn (9,98 phút) nên rất khó tổng hợp các hợp chất đánh dấu với 13N dùng trong nghiên cứu PET thường quy. Trong những năm 1970, người ta đã nêu ra những ích lợi của DCPX amonia [13N] (NH3 hoặc NH4+ dạng ion) dùng trong ghi hình tưới máu cơ tim. Do đó, việc sản xuất 13N phải tiến hành chiếu điều chế thành NH3[13N] trực tiếp ngay chính trong mẫu bia.
Phản ứng hạt nhân thông thường nhất là khi bắn phá proton (10 ¸ 15 MeV) vào hạt nhân bia 16O bền, tự nhiên ở dạng khí hoặc lỏng (nước). Khi 13N sinh ra trong bia, nó phản ứng với nước tạo thành dạng nitrate và ion nitrite. Sau đó thêm chất khử là titanium chloride vào nước trong bia sẽ sinh ra NH3[13N]. Với nguyên liệu bia trong áp suất cao, dung môi ethanol có thể được dùng trong bia và ethanol hoạt động như là một gốc tự do hydroxyl để cải thiện việc sản xuất NH3[13N].
- Sản xuất 15O:
Phản ứng hạt nhân thường dùng nhất là bắn phá deutron vào hạt nhân bia 14N có chứa 0,2 ¸ 0,5% oxygen sẽ tạo ra 15O trong dạng O2[15O]. Để sử dụng các proton có năng lượng thấp (10 ¸ 11 MeV), chất bia phải là khí 15N đã được làm giàu ở mức độ cao. Chất làm giá đựng bia thường được làm từ nhôm. Để sản xuất 15O dưới dạng CO2[15O] thì khí nitơ làm bia phải trộn với 2 ¸ 1,5% dioxit carbon. Bên cạnh bia, một nguồn khí nitơ chảy liên tục qua bia đến tủ hốt có chứa module tổng hợp nước được dùng, trong đó 15O sẽ kết hợp với khí H2 và chất xúc tác là palladi alumin trong nhiệt độ cao (300 ¸ 4000C) để sản xuất nước [15O].
- Các halogen phóng xạ phát positron:
Trong các halogen, 18F là đồng vị phóng xạ quan trọng nhất dùng trong PET. Các halogen khác như 75Br và 124I cũng có tiềm năng ứng dụng nhiều trong lâm sàng và có thể điều chế được trong máy gia tốc y học.
+ Sản xuất 18F:
Có 2 loại hạt nhân bia được dùng để sản xuất ra 2 dạng hóa học khác nhau của flourine. Dạng bia lỏng để sản xuất 18F kiểu ion ái nhân (nucleophilic: 18F–) và dạng bia gas để sản xuất 18F ở dạng khí 18F ái điện tử (electrophilic: F218F).
Phản ứng hạt nhân thông thường nhất được dùng để sản xuất 18F là ion Flouride dựa trên phản ứng bắn phá bằng proton vào các nguyên tử 18O dưới dạng nước rất giàu 18O làm nguyên liệu bia. Một giá chuẩn đựng nguyên liệu bia được làm bằng nhôm chứa 0,3 ¸ 3,0 ml nước dung dịch bia. Một vài Curries 18F được sinh ra dễ dàng trong thời gian 1 ¸ 2 giờ với việc bắn phá chùm proton có năng lượng 10 ¸ 19 MeV ở cường độ 20 ¸ 35 mA. Trong khi đó, theo lý thuyết khi SA của 18F là 1700 Ci/mmol thì NCA 18F được sinh ra thông thường là <10 Ci/mmol. Phản ứng hạt nhân thông thường nhất trong sản xuất 18F ở dạng khí là dựa vào việc bắn phá bằng deutron vào các nguyên tử 20Ne dưới dạng khí (neon tự nhiên). Một loại bia bằng hợp chất nickel (NiF) được nạp vào cùng với khí neon và với 0,1% khí F tự nhiên. Quá trình bắn phá diễn ra từ 1 ¸ 2 giờ với 8 ¸ 9 MeV của chùm deutron, thu được < 1,0 Ci F2[18F] với SA rất thấp (10 ¸ 20 mCi/ mmol). Một phương pháp “bắn kép” đã được phát triển để sản xuất khí 18F dựa trên bắn phá bằng proton vào 18O dưới dạng khí 18O đặt vào bia dạng khí. Sau chiếu xạ, 18F dính vào thành của lọ đựng bia. ống khí bia 18O được chuyển vào bình chứa khí argon trộn với 1% khí F lạnh. Sau thời gian chiếu xạ lần 2 khoảng < 10 phút sẽ sinh ra khí F2[18F]. Phương pháp này rất có lợi trong điều chế 18F ái điện tử bằng máy gia tốc với chùm proton duy nhất để bắn phá. Vì [18F]18F2 luôn được pha loãng với khí F2 lạnh (là chất mang), nên SA của 18F ái điện tử là rất thấp và không tối ưu về hoạt độ trong tổng hợp đánh dấu 18F làm DCPX có hoạt độ riêng cao dùng trong PET.
+ Sản xuất 75Br và 76Br:
Hai loại hạt nhân phóng xạ này thường được sinh ra do chùm proton bắn phá hạt nhân bia là 76Se dưới dạng Cu2Se giàu 76Se (96%) làm nguyên liệu bia. Rồi sau đó 76Br được tách ra từ bia rắn bằng khuếch tán nhiệt. T1/2 dài của 76Br (16,2 giờ) là lợi thế cho quá trình tổng hợp các DCPX và thương mại. Tuy nhiên, 76Br có sơ đồ phân rã phức hợp và phát positron năng lượng cao gây nên liều cao không có lợi cho bệnh nhân và công tác an toàn phóng xạ.
75Br có T1/2 tương đối ngắn (97 phút) có thể ưu việt hơn đối với việc phát triển DCPX PET. Một trong những phản ứng hạt nhân thông thường là 76S (p,2n) 75Br. Nhưng năng lượng tối ưu của proton phải là 18 ¸ 28 MeV và 75Br được tách ra từ bia rắn bằng phương pháp cất khô và bám vào bông Platin.
+ Sản xuất 124I:
Vì iod hóa các protein, peptid và các phân tử nhỏ diễn ra rất dễ dàng nên 124I có tiềm năng to lớn trong phát triển sản xuất DCPX dùng cho PET. Tuy nhiên, Tp của nó tương đối dài và phân rã phức tạp với một lượng năng lượng cao của positron làm cho hạt nhân phóng xạ này ít được dùng vì độc hại cho bệnh nhân.
Phương pháp dùng proton năng lượng thấp (15MeV) bắn phá vào các hạt nhân nguyên tử 124Te đã được làm giàu đang được phát triển. Nguyên liệu bia rắn gồm một dung dịch đặc có chứa oxid nhôm và oxid 124Te đã làm giàu. 124I được lấy ra từ bia bằng phương pháp cất khô. Iod phóng xạ bay hơi và bám vào ống thủy tinh Pyrex được phủ một lượng nhỏ hydroxid Na.
- Các kim loại phóng xạ phát positron (Ga, Y và Cu):
Sự phát triển các DCPX cho SPECT như Octreotide - 111In và Trodat - 99mTc đã được ứng dụng trong chẩn đoán lâm sàng, nó thuộc các loại peptid, các phân tử nhỏ và ngay cả những mảnh kháng thể đặc biệt với các receptor hay các kháng nguyên trên tế bào. Các chất này được đánh dấu hạt nhân phóng xạ thích hợp để làm DCPX. Một số hạt nhân phóng xạ phát positron thuộc các nguyên tố nhóm III (Ga, In và Y) có thể được sản xuất trong các máy gia tốc y học. Ngoài ra một số Generator có sẵn trong thị trường cũng sinh ra được một số kim loại phóng xạ con phát positron để dùng trong lâm sàng.
66Ga là hạt nhân phóng xạ có thời gian bán huỷ trung bình, phát positron năng lượng rất cao (4,1 MeV). Nó được sản xuất theo phản ứng bắn phá hạt nhân bia là 66Zn (p, n) 66Ga (Schlyer 2003). Sau phản ứng tạo ra 66Ga, chúng được tách ra khỏi hỗn hợp bia bằng phương pháp trao đổi ion hoặc chiết ra bằng dung môi.
Ytrium-86 cũng là một hạt nhân phóng xạ có thời gian bán rã trung bình, phát tia positron năng lượng cao (3,15 MeV). Hạt nhân phóng xạ này cũng được ứng dụng nhiều trong lâm sàng. Nó được đánh dấu vào các phân tử kháng thể, các peptid để nghiên cứu phân bố sinh học và đo liều phóng xạ. Trước khi điều trị bằng các thuốc phóng xạ đánh dấu 86Y, người ta thường phải nghiên cứu thăm dò trước với PET để thiết lập hồ sơ về khối u cần điều trị. 86Y được điều chế theo phản ứng 86Sr (p, n) 86Y. Các hạt nhân bia 86Sr thường được làm rắn và chứa trong lá mỏng hoặc các viên carbonat stronti. Sau bắn phá bia, 86Y thường được tách ra bằng cách cho tan vào dung dịch acid, rồi làm kết tủa và cuối cùng được tinh khiết bằng sắc ký trao đổi ion âm.
Có nhiều đồng vị của đồng cũng phát positron như 61Cu, 62Cu và 64Cu. Đặc biệt 64Cu phát positron năng lượng thấp như 18F, nên có thể dùng ghi hình với độ phân giải cao. Hơn nữa, nó có đời sống tương đối dài (12,7 giờ) cho nên rất thích hợp để sản xuất DCPX với protein và peptid để dùng cho PET. Nó được sản xuất theo phản ứng 64Ni (p, n) 64Cu. Hạt nhân bia chứa trong lá mỏng đã được làm giàu nickel. Sau phản ứng, 64Cu được tách ra bằng dung dịch acid và sắc ký trao đổi ion. Kỹ thuật sản xuất 61Cu cũng tương tự, nhưng bia là lá mỏng chứa 61Ni qua phản ứng hạt nhân 61Ni (n, p) 61Cu.