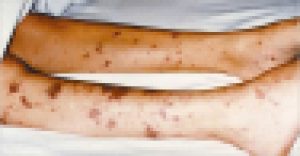
Điều trị 6 bệnh nhân (BN) viêm khớp dạng thấp (VKDT) đáp ứng không đầy đủ với methotrexat (MTX) bằng tocilizumab - TCZ (actemra) 8 mg/kg/tháng phối hợp với MTX 15 mg/tuần, theo dõi trong 3 tháng. Kết quả: số lượng khớp sưng, số lượng khớp đau, điểm VAS, tốc độ lắng hồng cầu, nồng độ CRP, các chỉ số đánh giá mức độ hoạt động bệnh đều giảm. Chỉ số DAS28 giảm < 3,2, đạt mục tiêu kiểm soát hoạt tính bệnh VKDT; không có BN nào xuất hiện các tác dụng ngoại ý như rối lipid máu, tăng men gan và nhiễm khuẩn.
* Từ khóa: Viêm khớp dạng thấp; Methotrexat; Tocilizumab.
The Effectiveness of Tocilizumab in Treatment of Rheumatoid Arthritis in Patients with Incomplete Response to Methotrexate
Summary
6 patients with rheumatoid arthritis (RA) who had an incomplete respone to MTX were treated with TCZ 8 mg/kg/month combined with MTX 15 mg/week for 3 months. The result showed that TCZ had high effects on decrease in swollen and tender joints, VAS, ESR, CRP and DAS index in RA. No patients had dislipidemia, hyper-hepatoenzyme and infection.
* Key words: Rheumatoid arthritis; Methotrexate; Tocilizumab.
ĐẶT VẤN ĐỀ
Viêm khớp dạng thấp là một bệnh khớp viêm mạn tính do cơ chế tự miễn dịch với tổn thương ban đầu đặc hiệu là viêm mạn tính màng hoạt dịch. Có nhiều cytokine liên quan tới cơ chế bệnh sinh của VKDT, trong đó người ta tìm thấy vai trò quan trọng của các cytokine như TNF, IL-1, IL-6 và IL-17.
Cho tới nay, nhiều nghiên cứu cho thấy hiệu quả của các thuốc chống thấp khớp làm thay đổi bệnh (Disease-Modifying Anti-Rheumatoid Arthritis - DMARDs) kinh điển trong điều trị VKDT; việc kết hợp MTX với hydroxychloroquin (HCQ), sulfasalazin (SSZ) cho thấy dung nạp tốt và hiệu quả hơn MTX đơn thuần [4, 10]. Tuy nhiên, khi kết hợp MTX với sulfasalazin (SSZ) và hydroxychloroquin (HCQ) được gọi là liệu pháp 3 thuốc vẫn có tới 30% BN không đáp ứng đầy đủ với trị liệu này. Hơn nữa, ở những BN phải dùng corticoid kéo dài dẫn đến nhiều tác dụng ngoại ý muốn, phụ thuộc liều, làm tăng gánh nặng bệnh tật và chi phí y tế [8].
Do vậy, trong những năm gần đây, việc sử dụng các tác nhân sinh học là một lựa chọn trong điều trị VKDT. Điều trị đích kháng cytokine là một phần quan trọng trong điều trị VKDT bằng tác nhân sinh học, cho thấy những kết quả khả quan trên lâm sàng, đặc biệt trên BN đáp ứng không đầy đủ với MTX. Cho đến nay, các thuốc kháng cytokine được sử dụng điều trị VKDT là kháng TNF, kháng IL-1 và kháng IL-6.
Tocilizumab là một kháng thể đơn dòng kháng thụ thể IL-6 của người tái tổ hợp, gắn với thụ cảm thể của IL-6 dạng hòa tan và trên màng tế bào, ức chế hoạt tính tiền viêm thông qua trung gian IL-6 [7]. Do nồng độ IL-6 huyết thanh liên quan hoạt tính bệnh VKDT, nên điều trị nhắm đích kháng thụ cảm thể của IL-6 bằng TCZ là một hướng tiếp cận lý tưởng trong điều trị VKDT.
Tocilizumab được chỉ định trong điều trị VKDT đáp ứng không đầy đủ với các DMARDs thường quy [6] cũng như ở BN VKDT thất bại với kháng TNF [5].
Tuy nhiên, ở Việt Nam, giá thành các thuốc sinh học quá cao so với thu nhập, việc sử dụng các tác nhân sinh học còn chưa nhiều. Vì vậy, hiệu quả, tính an toàn của TCZ trên người Việt Nam như thế nào là vấn đề cần phải nghiên cứu.
Khoa Khớp - Nội tiết, Bệnh viện Quân y 103 đã điều trị bằng TCZ cho BN VKDT đáp ứng không đầy đủ với MTX, có yếu tố tiên lượng nặng, hoặc thất bại với kháng TNF. Chúng tôi tiến hành nghiên cứu này với mục tiêu: Bước đầu đánh giá kết quả, tính an toàn của tocilizumab (actemra) trong điều trị VKDT ở BN thất bại với methotrexat.
ĐỐI TƯỢNG VÀ PHƯƠNG PHÁP NGHIÊN CỨU
1. Đối tượng nghiên cứu.
06 BN VKDT điều trị nội trú tại Khoa Khớp - Nội tiết, Bệnh viện Quân y 103 từ 3 - 2014 đến 10 - 2014 bằng TCZ (actemra) 8 mg/kg/tháng kết hợp với MTX 15 mg/tuần.
* Tiêu chuẩn lựa chọn BN:
+ Chẩn đoán VKDT theo ACR (1987) (American College of Rheumatology).
+ Đã điều trị bằng MTX với 15 mg/tuần trong thời gian 6 tháng.
+ Chưa đạt mục tiêu điều trị với DAS28 (CRP) > 3,2.
+ Không có chống chỉ định với TCZ.
* Tiêu chuẩn loại trừ:
+ BN đang dùng hoặc mới dừng sử dụng một tác nhân sinh học khác.
+ BN không đồng ý dùng TCZ.
+ BN xuất hiện nhiễm trùng nặng trong quá trình điều trị TCZ.
+ BN bỏ điều trị trước 3 tháng.
2. Phương pháp nghiên cứu.
Nghiên cứu mô tả, theo dõi dọc sau điều trị 1, 2, 3 tháng.
* Các chỉ tiêu theo dõi trước, trong và sau điều trị:
+ Các chỉ số lâm sàng: số lượng khớp đau, số lượng khớp sưng (28 khớp), điểm đau VAS (Visual Analoge Score), các chỉ số đánh giá hoạt tính bệnh (Disease Activity Score - DAS28), (C-reactive protein) - DAS28 (CRP), DAS28 (tốc độ lắng hồng cầu), (chỉ số hoạt động bệnh lâm sàng - CDAI), (chỉ số hoạt động bệnh đơn thuần - SDAI).
+ Các chỉ số cận lâm sàng: bilan lipid máu, AST, ALT, CRP, tốc độ lắng hồng cầu, hồng cầu, Hb, anti-CCP, RF (yếu tố thấp).
* Xử lý số liệu: theo chương trình thống kê SPSS 17.0.
KẾT QUẢ NGHIÊN CỨU VÀ BÀN LUẬN
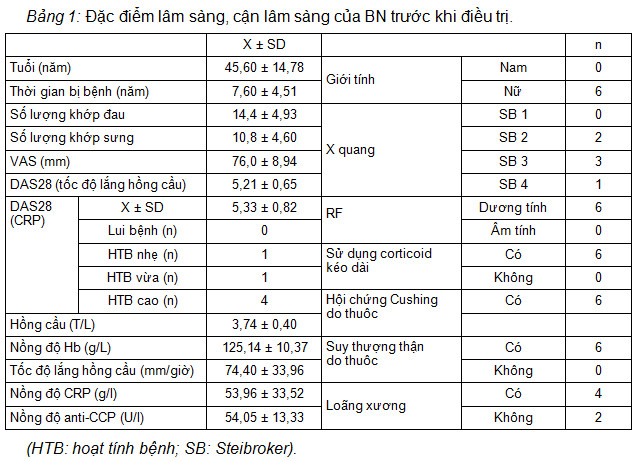
Cả 6 BN trong nghiên cứu là nữ, độ tuổi trung niên, yếu tố thấp và anti-CCP dương tính, điều này phù hợp với đặc điểm dịch tễ học của VKDT. Quá trình dùng corticoid kéo dài ở BN đều dẫn đến hội chứng Cushing và suy thượng thận do thuốc.
Mặc dù, BN được điều trị tối ưu bằng MTX, nhưng đều có số lượng khớp đau, số lượng khớp sưng, nồng độ CRP, tốc độ lắng hồng cầu và hoạt tính bệnh cao, hình ảnh hủy xương trên X quang, ngược lại nồng độ Hb lại thấp. Trong các chỉ số này, hoạt tính bệnh cao, hình ảnh hủy xương trên X quang là những yếu tố tiên lượng nặng cho phép chỉ định điều trị sinh học khi đáp ứng không đầy đủ với MTX.
Loãng xương làm tăng tỷ lệ tàn phế và tử vong ở BN VKDT. Ở BN VKDT có dùng corticoid, ngoài vai trò hoạt hóa hủy cốt bào của hệ thống RANKL/OPG/Wnt và các yếu tố nguy cơ khác như nữ giới, chế độ ăn thiếu canxi và vitamin D, sử dụng corticoid kéo dài, đây là một thực tế khó khắc phục ở Việt Nam. Điều trị bằng tác nhân sinh học như TCZ hy vọng kiểm soát hoạt tính bệnh, giảm liều và cắt corticoid, cải thiện mật độ xương. Tuy nhiên do nghiên cứu trong thời gian ngắn nên chúng tôi chưa đánh giá được thay đổi mật độ xương ở những BN này.
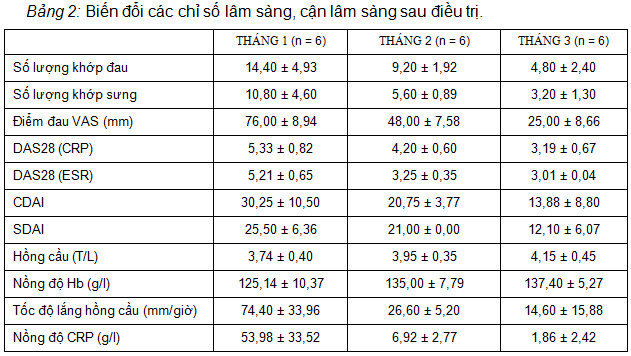
Sau điều trị 03 tháng, các chỉ số như số lượng khớp đau, số lượng khớp sưng, điểm đau VAS, nồng độ CRP, tốc độ lắng hồng cầu, các chỉ số kết hợp đánh giá mức độ hoạt động bệnh DAS28 (CRP/ESR), CDAI, SDAI đều giảm. Ngược lại, số lượng hồng cầu và nồng độ Hb tăng. Riêng chỉ số DAS28 (CRP/tốc độ lắng hồng cầu) giảm ≤ 3,2, đạt mục tiêu kiểm soát hoạt tính bệnh ở BN VKDT giai đoạn muộn.
Nghiên cứu của Maini RN và CS (2006) [9] trên 359 BN VKDT hoạt động đáp ứng không đầy đủ với MTX cho thấy giảm chỉ số DAS28 sau 4 tuần ở tất cả BN. Phần lớn BN điều trị với liều 8 mg/kg, nồng độ CRP và tốc độ lắng hồng cầu đều trở về giá trị bình thường. Từ đó, các tác giả đưa ra kết luận tác nhân kháng IL-6 có hiệu quả cao và là công cụ triển vọng trong giảm hoạt tính bệnh VKDT.
Ở Việt Nam, TCZ được sử dụng 05 năm nay, tuy nhiên số lượng BN chưa nhiều. Theo nghiên cứu của Đặng Hồng Hoa [1], Nguyễn Mai Hồng [2], Phan Văn Thuấn [3], TCZ (actemra) có hiệu quả cải thiện đặc điểm lâm sàng, cận lâm sàng ở BN VKDT tốt hơn rõ rệt so với trước khi điều trị.
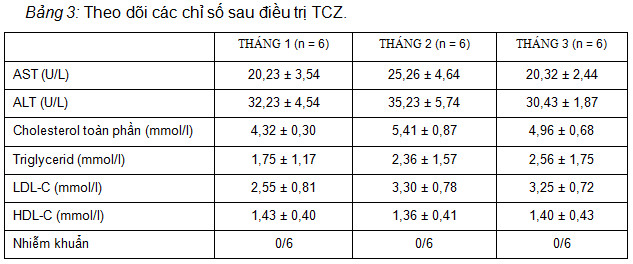
Trong 6 BN nghiên cứu, chúng tôi thấy không có sự biến đổi về tính chất bệnh lý nồng độ chỉ số lipid, men gan, không xuất hiện nhiễm khuẩn huyết, lao phổi. Tuy nhiên, do nghiên cứu với số lượng BN hạn chế, thời gian ngắn nên chưa thể nhận định một cách chính xác độ an toàn của TCZ ở người Việt Nam.
Maini RN và CS (2006) [9] thấy TCZ dung nạp tốt, có độ an toàn tương đương các tác nhân sinh học và thuốc ức chế miễn dịch khác. Sự biến đổi hình răng cưa của nồng độ AST và ALT (tăng lên và giảm xuống giữa các lần truyền); nồng độ cholesterol toàn phần và tryglicerid tăng có hồi phục, đồng thời giảm có hồi phục nồng độ HDL-C và bạch cầu trung tính, cả hai sự biến đổi ở mức độ trung bình; nhiễm khuẩn huyết gặp ở 2 BN điều trị phối hợp TCZ 8 mg/kg/tháng với MTX.
Đặng Hồng Hoa [1], Nguyễn Mai Hồng [2] và Phan Văn Thuấn [3], không gặp tác dụng không mong muốn nặng, không có BN nào phải ngưng điều trị.
KẾT LUẬN
Qua nghiên cứu 6 BN VKDT đáp ứng không đầy đủ với MTX điều trị phối hợp TCZ 8 mg/kg/tháng với MTX 15 mg/tuần, chúng tôi nhận thấy TCZ làm cải thiện các chỉ số lâm sàng như: số lượng khớp sưng, số lượng khớp đau, điểm VAS, các chỉ số đánh giá mức độ hoạt động của bệnh. Chỉ số cận lâm sàng đánh giá quá trình viêm cũng cải thiện rõ rệt: giảm tốc độ lắng hồng cầu; giảm nồng độ CRP. Sử dụng TCZ khá an toàn, không có tác dụng ngoại ý như tăng men gan, rối loạn lipid máu, nhiễm khuẩn trong thời gian 3 tháng điều trị.
TÀI LIỆU THAM KHẢO
1. Đặng Hồng Hoa. Bước đầu đánh giá hiệu quả và tính an toàn của tocilizumab (actemra) trong điều trị VKDT tại Bệnh viện E. Hội thảo Chuyên đề thuốc sinh học trong điều trị VKDT. Hội Thấp khớp học Việt Nam. 2012.
2. Nguyễn Mai Hồng. Bước đầu đánh giá hiệu quả và tính an toàn của tocilizumab (actemra) trong điều trị VKDT tại Bệnh viện Bạch Mai. Hội thảo Chuyên đề thuốc sinh học trong điều trị VKDT. Hội Thấp khớp học Việt Nam. 2012.
3. Phan Văn Thuấn. Đánh giá biến đổi lâm sàng, cận lâm sàng trong 12 tuần điều trị bệnh VKDT bằng phác đồ phối hợp tocilizumab (actemra) với methotrexate. Luận văn Thạc sỹ Y học, Học viện Quân y. 2014, pp.63.
4. Calguneri M, Pay S, Caliskaner Z et al. Combination therapy versus monotherapy for the treatment of patients with rheumatoid arthritis. Clin Exp Rheumatol. 1999, 17 (6), pp.699-704.
5. Emery P, Keystone E, Tony H P et al. L-6 receptor inhibition with tocilizumab improves treatment outcomes in patients with rheumatoid arthritis refractory to anti-tumour necrosis factor biologicals: results from a 24-week multicentre randomised placebo-controlled trial. Ann Rheum Dis. 2008, 67 (11), pp.1516-1523.
6. Genovese M C, McKay J D, Nasonov E L et al. Interleukin-6 receptor inhibition with tocilizumab reduces disease activity in rheumatoid arthritis with inadequate response to disease-modifying antirheumatic drugs: the tocilizumab in combination with traditional disease-modifying antirheumatic drug therapy study. Arthritis Rheum. 2008, 58 (10), pp. 2968- 2980.
7. Hirano T. Interleukin 6 and its receptor: ten years later. Int Rev Immunol. 1998, 16 (3-4), pp.249-284.
8. Huscher D, Thiele K, Gromnica-Ihle E. et al. Dose-related patterns of glucocorticoid-induced side effects. Ann Rheum Dis. 2009, 68 (7), pp.1119-1124.
9. Maini R N, Taylor P C, Szechinski J et al. Double-blind randomized controlled clinical trial of the interleukin-6 receptor antagonist, tocilizumab, in European patients with rheumatoid arthritis who had an incomplete response to methotrexate. Arthritis Rheum. 2006, 54 (9), pp.2817-2829.
10. Mottonen T, Hannonen P, Leirisalo-Repo M. et al. Comparison of combination therapy with single-drug therapy in early rheumatoid arthritis: a randomised trial. FIN-RACo trial group. Lancet. 1999, 353 (9164), pp.1568-1573.
Nguyễn Huy Thông*; Đoàn Việt Cường*; Nguyễn Minh Núi*
Nguyễn Ngọc Châu*; Nguyễn Thị Phi Nga*